下列关系式正确的是
A.常温下PH=2的甲酸与pH=12的烧碱溶液等体积混合: |
B.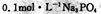 溶液中: 溶液中: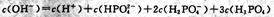 |
C.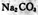 溶液加水稀释后,恢复至原温度,所有离子浓度均减小 溶液加水稀释后,恢复至原温度,所有离子浓度均减小 |
| D. 1L 0.3mol ?L-1NaOH溶液吸收标准状况下4. 48L CO2: |
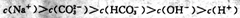
下列说法正确的是
| A.全部由非金属元素形成的化合物中只含有共价键 |
| B.分子晶体的熔点较低,因为分子晶体中有化学键 |
| C.金属在常温下都以晶体形成存在 |
| D.金属晶体中,自由电子几乎均匀分布在整个晶体中,被许多金属离子共用 |
R2O8n-离子在一定条件下可以把Mn2+离子氧化成MnO4-,若反应后R2O8n-离子变为RO42-离子。又知反应中氧化剂与还原剂的物质的量之比为5:2,则n的值是
| A.1 | B.2 | C.3 | D.4 |
根据反应(1)~(4),可以判断下列四种物质的氧化性由强到弱的正确顺序
(1)Cl2+2KI===2KCl+I2 (2)2FeCl2+Cl2===2FeCl3
(3)2FeCl3+2HI===2FeCl2+2HCl+I2 (4)H2S+I2=2HI+S
| A.H2S>I2>Fe3+>Cl2 | B.Cl2>Fe3+>I2>H2S |
| C.Fe3+>Cl2>H2S>I2 | D.Cl2>I2>Fe3+>H2S |
某物质的晶体中含A、B、C三种元素,它的排列方式如图(其中前后两面心上的B原子末画出)晶体中A、B、C的原子个数比为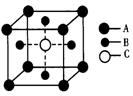
A.1:3:1 B.2:3:l C.1:2:1 D.1:3:3
在下列有关晶体的叙述中错误的是
| A.离子晶体中一定存在离子键 | B.原子晶体中只存在共价键 |
| C.原子晶体的熔沸点一定很高 | D.稀有气体的原子能形成原子晶体 |