下列实验现象预测正确的是( )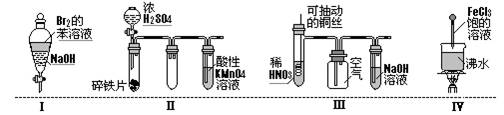
| A.实验I:振荡后静置,上层溶液颜色保持不变 |
| B.实验II:酸性KMnO4溶液中出现气泡,且颜色逐渐褪去 |
| C.实验III:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色 |
| D.实验IV:继续煮沸溶液至红褐色,停止加热,当光束通过体系时可产生丁达尔效应 |
在0.1mol/L的CH3COOH溶液中存在如下电离平衡: CH3COOH CH3COO-+H+,对于该平衡,下列叙述正确的是()
CH3COO-+H+,对于该平衡,下列叙述正确的是()
| A.加入少量NaOH固体,平衡向正反应方向移动 |
| B.加水,反应速率增大,平衡向逆反应方向移动 |
| C.滴加少量0.1mol/LHCl溶液,溶液中C(H+)减少 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
已知反应:① 2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol
② 稀溶液中,H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol
下列结论正确的是
| A.碳的燃烧热大于110.5 kJ/mol |
| B.①的反应热为221 kJ/mol |
| C.稀硫酸与稀NaOH溶液反应的中和热为57.3 kJ |
| D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ 热量 |
已知:C(s) + CO2(g)  2 CO(g);△H>0。反应达到平衡后,下列条件能使反应向正方向进行的是
2 CO(g);△H>0。反应达到平衡后,下列条件能使反应向正方向进行的是
| A.降低温度和减小压强 | B.升高温度和减小压强 |
| C.降低温度和增大压强 | D.升高温度和增大压强 |
已知反应2SO2(g)+O2(g) 2SO3(g),下列判断正确的是
2SO3(g),下列判断正确的是
| A.2 mol SO2和足量O2反应,必定生成2 mol SO3 |
| B.该反应在容积不变的密闭容器中,若混合气的密度不变,说明达到平衡状态 |
| C.平衡时,SO2消耗速率必定等于O2生成速率的两倍 |
| D.平衡时,SO2浓度必定等于O2浓度的两倍 |
已知H2(g)+Cl2(g)=2HCl(g)△H= -184.6kJ·mol-1, 则反应HCl(g)=1/2H2(g)+1/2Cl2(g)的△H为
| A.+184.6kJ·mol-1 | B.―92.3kJ·mol-1 |
| C.+92.3kJ | D.+92.3kJ·mol-1 |