某钠盐溶液中可能含有NO2-、SO42-、SO32-、CO32-、Cl-、I-等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色。
⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)2溶液,再滴加KSCN溶液,显红色
该同学最终确定在上述六种离子中共含NO2-、CO32-、Cl-三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
| A.①②④⑤ | B.③④ | C.③④⑤ | D.②③⑤ |
在实验室中,下列除去杂质的方法正确的是
| A.溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出溴 |
| B.乙烷中混有乙烯,通过氢气在一定条件下反应,使乙烯转化为乙烷 |
| C.硝基苯中混有浓HNO3和H2SO4,将其倒入到NaOH溶液中,静置,分液 |
| D.乙烯中混有SO2和CO2,将其通入溴水中洗气 |
由两种有机物组成的混合物,在一定温度和压强下完全汽化为气体,在同温同压下只要混合气体的体积一定,那么无论混合物以何种比例混合,它们完全燃烧时所消耗的氧气的体积也是一定的,符合这种情况的可能是
| A.乙醇和乙酸 | B.苯和苯甲酸(C7H6O2) |
| C.葡萄糖和鼠李糖(C6H12O5) | D.丙酮(C3H6O)和丙二醇(C3H8O2) |
制备一氯乙烷最好采用的方法是
| A.乙烷和Cl2取代 | B.乙烯和Cl2加成 |
| C.乙烯和HCl加成 | D.乙烯和H2加成后再与Cl2取代 |
下图是某有机物分子的比例模型,有关该物质的推断不正确的是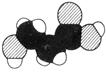
| A.分子中可能含有羟基 |
| B.分子中可能含有羧基 |
| C.分子中可能含有氨基(─NH2) |
| D.该物质的化学式可能为C3H6O3 |
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氯气中的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ。下列关系式中,正确的是
| A.Q1+Q2>Q3 | B.Q1+Q2<2Q3 |
| C.Q1+Q2<Q3 | D.Q1+Q2>2Q3 |