设C+CO2 2CO △H > 0 反应速率为 u1,N2+3H2
2CO △H > 0 反应速率为 u1,N2+3H2 2NH3 △H<0 反应
2NH3 △H<0 反应
速率为 u2,对于上述反应,当温度升高时,u1和u2的变化情况为
| A.同时增大 | B.同时减小 | C.增大,减小 | D.减小,增大 |
只用一种试剂就可区别NaCl、Al2(SO4)3、(NH4)2CO3、Mg(NO3)2四种溶液。这种试剂是
| A.NaOH | B.BaCl2 | C.AgNO3 | D.HCl |
由乙烯和乙醇蒸气组成的混和气体中,若碳元素的质量百分含量为60%,则氧元素的质量百分含量为()
| A.26.7% | B.15.6% | C.30% | D.无法确定 |
一定量的乙烷在氧气不足的情况下燃烧,得到CO、CO2和H2O的总质量为55.2g,若将产物通过浓H2SO4,浓H2SO4增重21.6g,则产物中CO的质量为
| A.2.8g | B.4. 4g | C.5.6g | D.8.8g |
以氯乙烷为原料制取乙二酸(HOOC-COOH)的过程中,要依次经过下列步骤中的:
①与NaOH的水溶液共热 ②与NaOH的醇溶液共热 ③与浓硫酸共热到170℃ ④在催化剂存在情况下与氯气加成 ⑤在Cu或Ag存在的情况下与氧气共热 ⑥与新制的Cu(OH)2共热
| A.①③④②⑥ | B.①③④②⑤ | C.②④①⑤⑥ | D.②④①⑥⑤ |
目前,世界上已合成了几百种有机超导体,TCNQ是其中之一。TCNQ的分子结构如下图所示。下列关于TCNQ说法错误的为 ()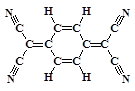
| A.分子中所有的氮原子在同一平面内 |
| B.属于芳香烃 |
| C.分子式为C12H4N4 |
| D.该物质难溶于水 |