可用于分离或提纯物质的方法有:①过滤 ②蒸馏 ③加热 ④分液(填序号)
(1)除去石灰水中悬浮的CaCO3颗粒
(2)除去NaCl晶体中混有的碘单质
(3)分离石油中各不同沸点范围的成分
(4)分离水和苯的混合物
Ⅰ.合成氨工业对化学和国防工业具有重要意义。写出氨的两种重要用途_________________________________。
Ⅱ.实验室制备氨气,下列方法中适宜选用的是__________________。
①固态氯化铵加热分解
②固体氢氧化钠中滴加浓氨水
③氯化铵溶液与氢氧化钠溶液共热
④固态氯化铵与氧化钙混合加热
Ⅲ.为了在实验室利用工业原料制备少量氨气,有人设计了如下装置(图119中夹持装置均已略去)。
图1-9
[实验操作]
①检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气产生。在F出口处收集氢气并检验其纯度。
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,继续通氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
完成下列问题:
(1)检验氢气纯度的目的是___________________________。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是__________________,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是___________________________,C瓶内气体的成分是_________。
(3)在步骤③中,先加热铁触媒的原因是____________________________________。反应管E中发生反应的化学方程式是___________________________。
制取氨气并完成喷泉实验(图中夹持装置均已略去)。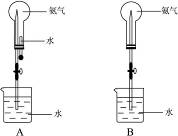
(1)写出实验室制取氨气的化学方程式:_________________________________________。
(2)收集氨气应使用___________法,要得到干燥的氨气可选用_____________作干燥剂。
(3)用图A装置进行喷泉实验,上部烧瓶已装满氨气,引发水上喷的操作是___________。该实验的原理是___________________。
(4)如果只提供如图B的装置,请说明引发喷泉的方法:___________________________。
实验室里若用下图装置制取氨气,请指出图中存在的问题,并简要说明如何改正。
存在问题:
改正方法:
某研究小组进行与NH3有关的系列实验。
(1)从下图中挑选所需仪器,画出制取干燥NH3的装置简图(添加必要的塞子、玻璃导管、胶皮管,固定装置和尾气处理装置不用画),并标明所用试剂。
(2)将NH3通入溴水中,有N2生成,反应的化学方程式为____________________。
(3)为验证“同温同压下,相同体积的任何气体都含有相同数目的分子”,该小组同学设计了如右图所示的装置,图中B管的容积是A管的2倍,活塞K1、K2、K3、K4、K5均关闭(固定装置和尾气处理装置略);HCl和NH3均不溶于石蜡油,也不与之反应;装置气密性好。
①在A管中充满与大气压强相等的干燥HCl气体。操作是________________。控制活塞K4、K5,调节C,使B管充满与A管同压的干燥NH3。
②缓缓开启K3,A管中的现象是___________________。要达到实验目的,当反应完成并恢复到室温时,B管中预期的现象是____________________;若观察不到预期现象,主要原因是____________________________________。
实验室模拟合成氨和氨催化氧化的流程如下:
已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从下图中选择制取气体的合适装置:氮气__________、氢气_________。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有_________、_________。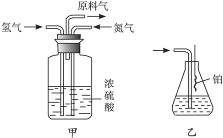
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨,_________(“会”或“不会”)发生倒吸,原因是____________________________________。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是___________________________,锥形瓶中还可观察到的现象是____________________________________。
(5)写出乙装置中氨氧化的化学方程式:___________________________。
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、_________、_________离子。