下列离子方程式正确的是
A.少量SO2通入Ca(ClO) 2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3 +2HClO +2HClO |
| B.氯化铁和铜反应:Fe3++Cu=Fe2++Cu2+ |
| C.石灰水与碳酸氢钠溶液混合:Ca2++CO32-=CaCO3↓ |
| D.硫酸氢钠溶液中加入氢氧化钡溶液至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X和Y组成原电池时,Y为电池的负极。X、Y、Z三种金属的活动性顺序为
| A.X>Y>Z | B.X>Z>Y | C.Y>X>Z | D.Y>Z>X |
下列反应不可用于设计原电池的是
| A.NaOH+HCl = NaCl+H2O |
B.2CH3OH+3O2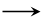 2CO2+4H2O 2CO2+4H2O |
| C.Zn+2HCl = ZnCl2+H2↑ |
| D.4Al+3O2+6H2O = 4Al(OH)3 |
对于放热反应2H2+O2====2H2O,下列说法正确的是
| A.产物H2O所具有的总能量高于反应物H2和O2所具有的总能量 |
| B.反应物H2和O2所具有的总能量高于产物H2O所具有的总能量 |
| C.反应物H2和O2所具有的总能量等于产物H2O所具有的总能量 |
| D.反应物H2和O2具有的能量相等 |
下列各组中属于同位素的是
| A.40K与40Ca | B.35Cl2和37Cl2 | C.D与T | D.金刚石与石墨 |
已知可逆反应2SO2+O2 2SO3是放热反应,下列说法正确的是
2SO3是放热反应,下列说法正确的是
| A.2molSO2 与1molO2 能完全反应生成2molSO3 ,升高温度可以加快此反应的化学反应速率 |
| B.2molSO2 与1molO2不能完全反应生成2molSO3,升高温度可以加快此反应的化学反应速率 |
| C.2molSO2 与1molO2 能完全反应生成2molSO3 ,升高温度减慢此反应的化学反应速率 |
| D.2molSO2 与1molO2 不能完全反应生成2molSO3 ,升高温度减慢此反应的化学反应速率 |