关于右图所示①、②两个装置的叙述,正确的是( )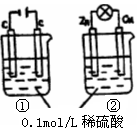
| A.装置名称:①是原电池,②是电解池 |
| B.硫酸浓度变化:①增大,②减小 |
| C.电极反应式:①中阳极:4OH- -4e- = 2H2O+O2↑②中正极:Zn -2e- = Zn2+ |
| D.离子移动方向:①中H+ 向阴极方向移动②中H+向负极方向移动 |
下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是
①NaHCO3 ②Al2O3 ③Al(OH)3④Al⑤NaAlO2
| A.③④ | B.②③④ | C.①②③④ | D.全部 |
钠在空气中发生变化的过程是
| A.Na→Na2O2→NaOH→Na2CO3·10H2O→Na2CO3 |
| B.Na→Na2O→NaOH→Na2CO3·10H2O→Na2CO3 |
| C.Na→Na2O2→NaOH→Na2CO3→NaHCO3 |
| D.Na→Na2O→NaOH→Na2CO3→NaHCO3 |
随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是
| A.无水硫酸铜、蔗糖 | B.硅胶、硫酸亚铁 |
| C.食盐、硫酸亚铁 | D.生石灰、食盐 |
高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇: ,若在温度和容器相同的三个密闭容器中,按不同方式投人反应物,测得反应达到平衡吋的有关数据如下表,则下列关系正确的是
,若在温度和容器相同的三个密闭容器中,按不同方式投人反应物,测得反应达到平衡吋的有关数据如下表,则下列关系正确的是
| A.a1+a3=1 | B.2Q1=Q3 | C.c1=c2 | D.2a1=a3 |
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) 2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
2C(g),达到平衡后,在不同的时间段,分别改变影响反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如下图所示:
下列说法中正确的是
| A.30~40 min间该反应使用了催化剂 |
| B.反应方程式中的x=1,正反应为吸热反应 |
| C.8 min前A的平均反应速率为0.08 mol·L-1·min-1 |
| D.30 min时降低温度, 40 min时升高温度 |