为了探究“水的净化”过程,某实验小组从河中取了水样,观察到:
A. 水样呈黄色,有异味 B.水样浑浊,有固体小颗粒。
现对水样进行如下处理:
(1)向水样中加入明矾搅拌溶解,静置一段时间后,进行 (填操作名称),除去固体小颗粒,在此操作中,玻璃棒所起的作用是 。
再向滤液中加入活性炭,利用其 性除去水样中的颜色和异味,该过程属于
变化(填“物理”或“化学”)
(2)若过滤结束,发现滤液仍然浑浊,可能的原因是
① ② 。
(3)同学们想知道所得滤液中是否溶解了某些固体物质,可接着对滤液进行 (填
操作方法)。
实验室现有下列仪器和用品,要进行该操作,必须用到的是(填序号) 。
①试管 ②铁架台(带铁圈) ③烧杯 ④酒精灯 ⑤滤纸 ⑥玻璃棒 ⑦量筒 ⑧蒸发皿
通过一年的化学学习,你已经掌握了实验室制取气体的一些规律,以下是老师提供的一些实验装置,请你结合下图回答问题: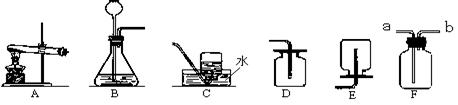
(1)写出实验室用A装置制取氧气的化学方程式 ;
反应类型是。
(2)利用上面的装置制取二氧化碳气体,你选择的装置按合理的顺序从左到右排列为,若用F装置干燥二氧化碳气体,进气口为,瓶内盛放的干燥剂为。
(3)已知氨气是一种密度比空气小且极易溶于水的气体。加热氯化铵与氢氧化钠的固体混合物制取氨气,应选择的发生装置是,理由;选择的收集装置是,理由是。
某品牌纯碱中含有少量氯化钠。某化学探究小组为了测定该品牌纯碱的纯度(即碳酸钠的质量分数),组内一同学设计如图所示实验: 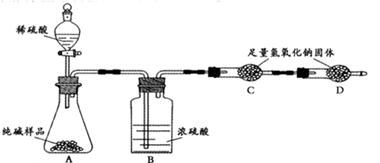
(1)A装置中反应的化学方程式为 。
(2)B装置的作用是 ;C装置中反应的化学方程式为。
(3) D装置的作用是 。
(4)小明提出能否用盐酸代替硫酸?同学们经过讨论认为不能,理由是。
(5)小华提出,要使测定结果更准确,应把A装置改成图15所示装置,并在反应前鼓入空气,其目的是_____________________;反应后还要鼓入空气,其目的是_____________________.
(6)称得纯碱样品的质量为12.0 g,实验前、后C装置(包含药品)的质量分别为61.2 g和65.6 g,则该纯碱样品的纯度为 %(精确到0.1%)。
结合图所示实验装置回答问题: 
(1) B装置由导管、橡皮塞、和 组成。
(2)实验室若用高锰酸钾制较干燥氧气,反应的化学方程式______________________,可选用的发生和收集装置是____________(填标号)。实验过程中,若发现试管破裂了,可能的原因是____________________________(写一点)。
(3)装置B与D组合,可以制取的一种气体是____________,反应的化学方程式______________________;能用D装置收集该气体的原因是___________________________。用D装置收集该气体,当观察到__________________时,才能把导气管放入集气瓶中。
小强同学看到妈妈将买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡。为了解其反应过程,他与学习小组的同学进行了如下探究。
【探究一】小组同学根据所学的化学知识设计并进行了如图所示的实验。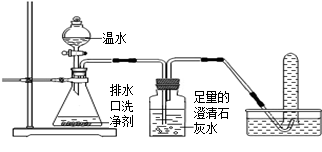
A B C
实验中观察到如下现象:A中有气泡产生;B中的澄清石灰水变浑浊;C中收集到的气体能使燃着的木条燃烧更旺。由此同学们得出结论:生成的两种气体分别是:(填化学式)。B中有关反应的化学方程式是。
【探究二】
(1)实验过程:
教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究: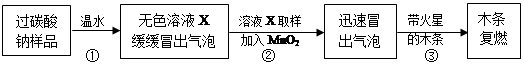
(2)提出问题:无色溶液X中的溶质有哪些物质?
(3)猜想与假设: 根据以上实验现象,X溶液中一定存在的溶质是;还可能存在Na2CO3、NaHCO3、NaOH中的一种或几种。
(4)查找资料:
资料1:氯化钙溶液呈中性;氯化钙溶液与碳酸氢钠溶液混合不发生反应;
氯化钙溶液与碳酸钠溶液混合后发生如下反应:Na2CO3 + CaCl2 ═ CaCO3↓ + 2NaCl。
资料2:NaHCO3溶液呈碱性,与石灰水反应生成白色沉淀;碳酸氢钠、碳酸钠与足量的酸反应产物相同。
(5)实验过程:小组同学对溶液X中的溶质进行了如下实验。请将下列实验方案填写完整。
| 实验操作 |
主要实验现象 |
结论 |
| ① |
证明溶液中有Na2CO3 |
|
| ② |
证明溶液中无NaHCO3 |
|
| ③ |
证明溶液中无NaOH |
(6)实验反思:根据资料,NaHCO3溶液能与石灰水反应生成白色沉淀。于是,同学们猜想:碳酸氢钠与氢氧化钠是否可以发生(写方程式)这样的反应?于是,同学们进行了新的探究实验。
下图是某同学设计的二氧化碳制取实验的微型一体化装置图,该装置的气密性良好。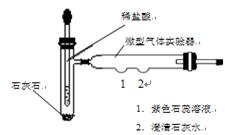
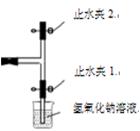
(1)关闭止水夹1,打开止水夹2,挤压胶头,滴入稀盐酸,生成的二氧化碳在微型气体实验器内与1、2处的溶液反应。1处紫色的石蕊溶液变成红色,2处的反应现象是。
(2)关闭止水夹2,打开止水夹1,再次挤压胶头,一段时间后,观察到烧杯中的现象是 。这是由于 (用化学方程式表示)的缘故。
(3)有同学认为:二氧化碳能溶于水并与水反应,因此实验(2)出现的现象不足以证明是二氧化碳和氢氧化钠发生了反应。那么,如何利用化学方法证明二氧化碳和氢氧化钠发生了反应?该实验方案是。