在没有氧气存在时,铁与水几乎不反应,但高温下,铁能与水蒸气反应。某同学利用铁与水蒸气反应后的固体物质进行了如下实验:
(1) 铁粉与水蒸气反应的化学方程式是:
(2)证明还原铁粉与水蒸气发生了反应的方法是
(3)固体溶于稀盐酸的化学方程式为 。
(4)试剂1的化学式是 。
(5)加入新制氯水后溶液红色加深的原因是(用离子方程式表示)
;
(6)某同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究。
①提出假设:
假设1:溶液中的+3价铁被氧化为更高的价态;
假设2: ;
②设计方案:
为了对你所提出的假设2进行验证,实验方案是
。
如图所示,在实验室里,通常利用浓硫酸与乙醇混合加热制乙烯: CH3CH2OH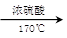 CH2=CH2↑+H2O,加热一段时间后溶液中有黑色现象出现。过一段时间后,经硫酸酸化的高锰酸钾溶液褪色。经分析得知:产生的气体中含有CH2=CH2、SO2、CO2、H2O。
CH2=CH2↑+H2O,加热一段时间后溶液中有黑色现象出现。过一段时间后,经硫酸酸化的高锰酸钾溶液褪色。经分析得知:产生的气体中含有CH2=CH2、SO2、CO2、H2O。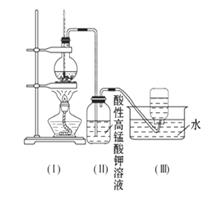
酸性高锰酸钾溶液褪色,甲同学认为能证明乙烯被酸性高锰酸钾溶液氧化了;乙同学认为不能证明乙烯被酸性高锰酸钾溶液氧化了。
(1)你认为哪个同学的观点正确? _____ (填“甲”或“乙”),理由是(从下列选项中选)_____
| A.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,能证明乙烯发生了氧化反应 |
| B.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,能证明乙烯发生了加成反应 |
| C.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,不能证明通入的气体是纯净物 |
| D.(Ⅱ)瓶中酸性高锰酸钾溶液褪色,只能证明通入的气体一定具有还原性 |
(2)丙同学取(Ⅱ)瓶中少量溶液于试管里,加入盐酸和氯化钡溶液,产生白色沉淀,他认为乙烯中一定混有二氧化硫,你认为他的结论是否可靠? _____ (填“可靠”或“不可靠”);理由是_____________________ 。
(3)丁同学想证明乙烯能否与溴发生反应,于是对上述实验进行了改进,改进的方法是:在装置(Ⅰ)和(Ⅱ)之间增加一个装有足量_____的洗气瓶,且将(Ⅱ)瓶中溶液换成_____ 。发生加成反应的化学方程式为
某研究小组利用下图装置探究温度对
还原
的影响(固定装置略)
(1)
的分解产物为。
(2)装置
的作用是,处理尾气的方法为。
(3)将研究小组分为两组,按图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置
加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。
| 步骤 |
操作 |
甲组现象 |
乙组现象 |
| 1 |
取黑色粉末加入稀盐酸 |
溶解,无气泡 |
溶解,有气泡 |
| 2 |
取步骤1中溶液,滴加
溶液 |
蓝色沉淀 |
蓝色沉淀 |
| 3 |
取步骤1中溶液,滴加
溶液 |
变红 |
无现象 |
| 4 |
向步骤3溶液中滴加新制氯水 |
红色褪去 |
先变红,后褪色 |
①乙组得到的黑色粉末是;
②甲组步骤1中反应的离子方程式为;
③乙组步骤4中,溶液变红的原因为;溶液褪色可能的原因及其验证方法为;
④从实验安全考虑,题9图装置还可采取的改进措施是。
利用废旧锌铁皮制备磁性
胶体粒子及副产物
。制备流程图如下:
已知:
及化合物的性质与
及化合物的性质相似。请回答下列问题:
(1)用
溶液处理废旧锌铁皮的作用有。
| A. | 去除油污 | B. | 溶解镀锌层 | C. | 去除铁锈 | D. | 钝化 |
(2)调节溶液
的
可产生
沉淀,为制得
,后续操作步骤是。
(3)由溶液
制得
胶体粒子的过程中,须持续通入
,原因是。
(4)
胶体粒子能否用减压过滤发实现固液分离?(填"能"或"不能"),理由是。
(5)用重铬酸钾法(一种氧化还原滴定法)可测定产物
中的二价铁含量。若需配制浓度为0.01000
的
标准溶液250
,应准确称取
(保留4位有效数字,已知
=294.0
)。
配制该标准溶液时,下列仪器中不必要用到的有。(用编号表示)。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管
(6)滴定操作中,如果滴定前装有
标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则测定结果将(填"偏大"、"偏小"或"不变")。
氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌(含有
(Ⅱ),
(Ⅱ),
(Ⅱ)等杂质)的流程如下:
提示:在本实验条件下, (Ⅱ)不能被氧化,高锰酸钾的还原产物是
回答下列问题:
(1)反应②中除掉的杂质离子是,发生反应的离子方程式为。
加高锰酸钾溶液前,若pH较低,对除杂的影响是。
(2)反应③的反应类型为,过滤得到的滤渣中,除了过量的锌外还有。
(3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是。
(4)反应④中产物的成分可能是
.取干操后的滤饼11.2
,煅烧后可得到产品8.1
. 则
等于。
正丁醛是一种化工原料。某实验小组利用如下装置合成正丁醛。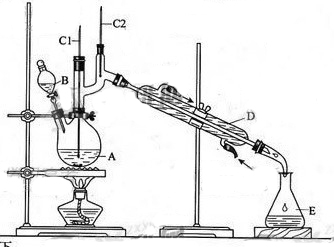
发生的反应如下:
反应物和产物的相关数据列表如下:
| 沸点/℃ |
密度/(
) |
水中溶解性 |
|
| 正丁醇 |
11.72 |
0.8109 |
微溶 |
| 正丁醛 |
75.7 |
0.8017 |
微溶 |
实验步骤如下:
将6.0
放入100
烧杯中,加30
水溶解,再缓慢加入5
浓硫酸,将所得溶液小心转移至
中。在
中加入4.0
正丁醇和几粒沸石,加热。当有蒸汽出现时,开始滴加
中溶液。滴加过程中保持反应温度为90-95℃,在E中收集90℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75-77℃馏分,产量2.0
。
回答下列问题:
(1)实验中,能否将
溶液加到浓硫酸中,说明理由。
(2)加入沸石的作用是。若加热后发现未加沸石,应采取的正确方法是。
(3)上述装置图中,
仪器的名称是,
仪器的名称是。
(4)分液漏斗使用前必须进行的操作是(填正确答案标号)。
a.润湿 b.干燥 c.检漏 d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在层(填"上"或"下")
(6)反应温度应保持在90-95℃,其原因是。
(7)本实验中,正丁醛的产率为%。