下列有关化学用语错误的是
A.Na+的基态电子排布图是: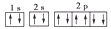 |
B.H2O分子的电子式为: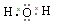 |
| C.Ca2+离子基态电子排布式为:1s22s22p63s23p6 |
D.氯原子结构示意图为: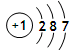 |
下图为元素周期表的局部,A、B、C、D为周期表中短周期元素,已知A原子最外电子层上的电子数是其次外层的一半。据此判断下列正确的是
| B |
D |
||
| A |
C |
A.A位于第2周期1A族 B.B的最高价氧化物的水化物是弱酸
C.原子半径A>C>B>DD.气态氢化物的热稳定性B>D>C>A
决定主族元素在元素周期表中所处位置的是该元素原子的
| A.质量数 | B.中子数 |
| C.最外层电子数 | D.电子层数和最外层电子数 |
下列各组离子中,能在溶液中大量共存的是
| A.Ba2+、Na+、SO42- | B.H+、Cl一、CO32- |
| C.Na+、Cu2+、Cl一 | D.Mg2+、K+、OH- |
水的净化常用到下列物质,其中用做凝聚剂而不能消毒的是
| A.明矾 | B.活性炭 | C.漂白粉 | D.臭氧 |
下列物质溶于水中,既破坏离子键又破坏共价键的是
| A.HCl | B.NaHSO4 | C.C2H5OH | D.NaOH |