短周期元素甲和乙,甲原子的最外层电子数为a,次外层电子数为b;乙原子的M层电子数为(a – b – 1),L层电子数为(a + b)。则甲、乙两元素形成的化合物具有的性质是
①与水反应 ②与硫酸反应 ③与氢氧化钠溶液反应 ④与氯气反应
| A.①② | B.②③ | C.②④ | D.③④ |
某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②沼气和水煤气都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体。上述说法正确的是()
| A.①②③④ | B.①②⑤⑥ | C.③⑤⑥⑦ | D.①③④⑦ |
下图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是()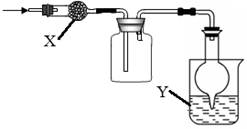
| 选项 |
X |
收集气体 |
Y |
| A |
碱石灰 |
氯化氢 |
水 |
| B |
碱石灰 |
氨气 |
水 |
| C |
氯化钙 |
二氧化硫 |
氢氧化钠 |
| D |
氯化钙 |
一氧化氮 |
氢氧化钠 |
某气体的水溶液呈酸性,该气体能使酸性高锰酸钾溶液褪色,也能使溴水褪色并出现浑浊,该气体是()
| A.HBr | B.SO2 | C.H2S | D.CO2 |
下列措施不合理的是()
| A.用SO2漂白纸浆和草帽辫 |
| B.用硫酸清洗锅炉中的水垢 |
| C.高温下用焦炭还原SiO2制取粗硅 |
| D.用 Na2S作沉淀剂,除去废水中的Cu2+和Hg2+ |
下列各组离子一定能大量共存的是()
| A.在含有大量[Al(OH)4]-的溶液中:NH4+、Na+、Cl-、H+ |
| B.在强碱溶液中:Na+、K+、CO32-、NO3- |
| C.在pH=12的溶液中:NH4+、Na+、SO42-、Cl- |
| D.在c(H+)=0.1mol·L-1的溶液中:K+、I-、Cl-、NO3- |