、过碳酸钠(Na2CO4)在洗涤、印染、造纸、医药卫生等领域有大量应用。
已知:过碳酸钠与硫酸溶液反应的化学方程式如下: Na2CO4 +H2SO4 →Na2SO4 +H2O2 + CO2↑  2H2O2 →2H2O+ O2↑.为测定已变质的过碳酸钠(含碳酸钠)的纯度,设计如图所示的实验:Q为—具有良好的弹性的气球(不与反应物和生成物反应),称取一定量的样品和少量二氧化锰放于其中,按图安装好实验装置,打开分液漏斗的活塞,将稀H2SO4滴入气球中。
2H2O2 →2H2O+ O2↑.为测定已变质的过碳酸钠(含碳酸钠)的纯度,设计如图所示的实验:Q为—具有良好的弹性的气球(不与反应物和生成物反应),称取一定量的样品和少量二氧化锰放于其中,按图安装好实验装置,打开分液漏斗的活塞,将稀H2SO4滴入气球中。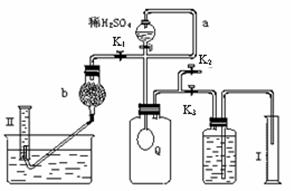
⑴Q内发生反应生成的气体为__________,导管a作用是 。
⑵为测出反应时生成气体的总体积,滴稀H2SO4前必须关闭K1、K2,打开K3。当上述反应停止,将K1、K2、K3处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是_________ _____,b中装的碱石灰的作用是_ _________________。
_________________。
⑶实验结束时,量筒I中有xmL水,量筒Ⅱ中收集到ymL气体(上述体积均已折算到标准状况),则过碳酸钠的纯度是____________
⑷某同学实验测得的过碳酸钠的纯度超过100%,你认为可能的原因是_______
| A.气体滞留在Q和导气管中,未全部进入量筒Ⅱ |
B.量筒Ⅱ读数时 ,量筒液面高于水槽液面 ,量筒液面高于水槽液面 |
| C.右侧量筒Ⅰ和储液集气瓶连接导管内的液体没有计入读数x |
| D.气体体积数值x、y没有扣除滴加的硫酸的体积 |
为研究浓硫酸的性质,某同学进行如下实验:
(1)称取铁和碳固体混合物12.0g放入30.0mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。取896mL(标准状况)气体Y通入足量溴水中,发生反应:
SO2+Br2+2H2O=2HBr+H2SO4然后加入足量BaCl2溶液,经适当操作后得到干燥固体4.66g。据此推知气体Y 中SO2的体积分数为 。
(2)分析上述实验中SO2体积分数的结果,该同学认为气体Y中还可能含有H2和CO2
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。
①写出产生CO2的化学方程式 。
②装置A中试剂的作用是 ,装置B的作用是 。
③简述确认气体Y中含有CO2的实验现象 。如果气体Y中含有H2,预计实验现象应是 。
Ⅰ.铁是人体必需的微量元素,绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。
(1)测定绿矾样品含量的实验步骤:
A.称取5.7 g样品,溶解配成 250 mL溶液
B.量取25 mL待测液于锥形瓶中
C.用硫酸酸化的0.01 mol/L KMnO4溶液滴定至终点,消耗KMnO4溶液体积为40 mL。
根据上述步骤回答下列问题:
①用硫酸酸化的KMnO4溶液滴定终点的标志是____________________。
②计算上述样品中 FeSO4·7H2O的质量分数为____________________。
Ⅱ.硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,常用于代替硫酸亚铁。
(2) 为检验分解产物的成分,设计如下实验装置进行实验,加热A中硫酸亚铁铵至分解完全。
①A中固体充分加热较长时间后,通入氮气,目的是_________________。
②装置B中BaCl2溶液的作用是检验分解产物中是否有SO3气体生成,若含有该气体,观察到的现象为________________。
③实验中观察到C中有白色沉淀生成,则C中发生的反应为______________(用离子方程式表示)。
某校化学实验兴趣小组为了探究实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如下图所示的实验装置(支撑用的铁架台省略),完成下列问题。
(1)用 MnO2和浓盐酸混合共热制得氯气的化学方程式是__________________;
(2)若用含有0.2mol HCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积在标准状况下总是小于1.12L的原因是__________________;
(3)①装置B的作用是__________________;
②装置D和E出现的不同现象说明的问题是__________________;
③装置F的作用是__________________;
④装置G中发生反应的化学方程式为__________________。
用如下图所示装置证明浓硫酸的强氧化性,并检验产物的性质。请回答:
(1)装置①中反应的化学方程式_______________________。
(2)装置②中的现象是_______________________。
(3)装置③中的现象可证明SO2有______________性。
(4)装置④中反应的离子方程式_________________。
(5)装置⑤的作用是____________________。
某课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下3 组实验,如图Ⅰ~III 所示。
(1)Ⅰ所示的实验,若固体质量相同且稀盐酸足量时,气球鼓起较小的是___________(填化学式)。
(2)II、III 所示的实验均能鉴别这两种物质,相关反应的化学方程式是①_____________、②_________________。
③与II 相比, III 的优点是______________________(填选项序号)。
a.III 比II 复杂
b.III 比II 安全
c.III 可以做到用一套装置同时进行两个对比实验,而II 不行
(3)若用III 验证碳酸钠和碳酸氢钠的热稳定性,则试管B 中装入的固体应该是_______________。