全球能源生产正向"氢能经济"转型,以可再生生物资源(如纤维素等)为原料生产氢气已成为能源研究的重点。下图是某新型能源转换与利用模式示意图。

(1)该模式中涉及的能源转化依次为:太阳能→生物质能→氢能→能;
(2)某有机物水相重整制取
分两步进行反应,其中第一步反应可表示为:
(未配平),则x:z== ;
(3)该系统中循环使用的物质是;
(4)氧氧燃料电池工作时,
和
在常温下反应.写出该反应的化学方程式:;
(5)与电解水相比.该模式制取氢气的主要优点是: .
2007年化学家格哈德·埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨(NH3)的反应过程,获得当年的诺贝尔化学奖。N2和H2合成氨的反应过程可用下图表示
(用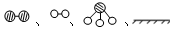 分别表示N2、H2、NH3 、在催化剂表面)
分别表示N2、H2、NH3 、在催化剂表面)
(1)图中表示的合成氨反应过程的顺序为:E→()→()→()→C(在括号中填写其它三张图示的字母);
(2)某研究性学习小组利用下图所示装置进行“分子的基本性质”的实验探究(实验过程中整套装置及有关气体均保持干燥)。
Ⅰ.在集气瓶B中充满氯化氢气体,K3处于关闭状态至操作Ⅱ完成为止;
Ⅱ.通过调节活塞K1、K2,在集气瓶A中充满氨气(氨气的密度小于空气),其操作是:打开K1、K2,在(选填“K1”或“K2”)处导管口通入氨气;
Ⅲ.集满氨气后,关闭K1、K2,再打开K3,一段时间后两只集气瓶中都出现白烟(白烟是氯化氢气体与氨气反应产生氯化铵固体的细小颗粒)。
①如果这两个瓶子是质地较软的塑料瓶,我们最终将会观察到__________________,原因是。
现有下列实验装置图,结合该图回答下列问题。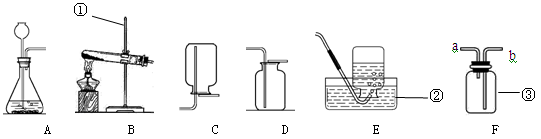
(1)写出图中标号仪器的名称:③。
(2)实验室采用分解过氧化氢溶液的方法来制取氧气,可以选用的发生装置为(填装置序号),发生反应的文字表达式为,若用F装置通过排水法来收集氧气,F装置的处理。
(3)若用加热高锰酸钾的方法制取氧气,则可选用的装置组合为,在固定试管时,试管口必须,这是为了。
(4)通过查阅资料得知:①氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,其水溶液称为氨水;②氨水能使无色酚酞试液变红;③实验室用氯化铵(NH4Cl)和熟石灰两种固体反应物混合加热可制取氨气,同时生成氯化钙和水。则实验室制取氨气的装置组合可以选用。小芳将收满氨气的集气瓶倒扣在滴有无色酚酞的水中,观察到的现象是__________________、________。
请用文字或化学符号表示下列化学反应,并在括号内标明该反应的基本反应类型。
(1)红磷在空气中燃烧,()反应;
(2)氯酸钾与二氧化锰共热,()反应;
(3)氢气在氯气中燃烧生成氯化氢。
(7分)(1)请用合适的化学用语(数字以及化学符号)填空:
①金元素;
②构成氯化钠的微粒是;
③2个硝酸根离子;
④由8个硫原子构成的分子;
(2)化学是一门以实验为基础的科学。图1~2是教科书上有关实验的装置图:
①图1是利用足量红磷燃烧来测定空气中氧气的含量。通过此实验可以得出的结论是:。
②图2是电解水实验。用化学符号表示此实验发生化学反应的式子是。通电一段时间后切断电源,用燃着的木条分别在两个玻璃管尖嘴口检验反应产生的气体,其中负极端的玻璃管内产生气体的检验现象是 。
京沪高速上,一辆槽罐车上满载的液态氯气快速泄漏,由于与事故发生地相距300m的地方是村庄,因此,此次液氯泄漏导致数十人死亡。信息链接:①氯气为黄绿色气体;②有强烈刺激性气味;③在常温下,氯气可溶于水,在高压下可以液化,并装入槽罐车中进行运输;④氯气密度为3.21g/L(空气为1.293g/L);⑤氯气可与氢气等非金属单质反应;⑥也可与钠、镁等金属单质反应;⑦还能与氢氧化钙反应生成次氯酸钙Ca(ClO)2、氯化钙和水。
(1)①-⑦中,属于氯气物理性质的是(填序号);
(2)请说明储存氯罐内温度升高是否会引发爆炸,为什么?
(3)写出氯气和氢氧化钙反应的符号表达式:。