一定温度下,可逆反应A(s)+2B(g) 2C(g)+D(g);△H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。
2C(g)+D(g);△H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。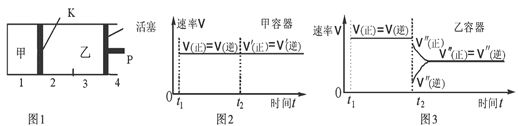
下列说法正确的是
| A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
| C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.保持活塞位置不变,改变温度,达到新的平衡后,甲、乙中B的体积分数均增大 |
下列实验装置、选用的试剂或实验操作中,都正确的是
| A.实验室用装置A制取氨气 | B.用B装置吸收氨气,并防止倒吸 |
| C.用C装置稀释浓硫酸 | D.用D装置除去CO2中的HCl |
短周期元素X、Y、Z在元素周期表中的位置如右下图所示,下列说法正确的是 ( )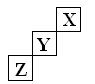
| A.X、Y、Z三种元素中,X的非金属性最强 |
| B.常压下X的单质的熔点比Z的低 |
| C.Y的最高正化合价为+7 |
| D.Y的氢化物的稳定性比Z的弱 |
在下列溶液中一定能大量共存的离子组是
| A.pH=2的溶液:Fe2+、NH4+、Cl—、NO3— |
B.能使pH试纸变深蓝色的溶液:Na+、 、S2—、CO32— 、S2—、CO32— |
| C.含有大量Fe3+的溶液:SCN—、I—、K+、Br— |
| D.澄清透明的无色溶液:ClO—、MnO4—、Al3+、SO42— |
下列离子方程式的书写不正确的是
| A.氢氧化钡溶液与稀硫酸反应:Ba2++SO42—+H++OH—=BaSO4↓+H2O |
| B.Ca(ClO)2溶液中通入过量CO2:ClO—+H2O+CO2=HCO3—+HClO |
| C.铜溶于稀硝酸:3Cu+8H++2NO3—=3Cu2++2NO↑+4H2O |
| D.将AlCl3溶液滴入氨水中:3NH3·H2O+Al3+=Al(OH)3↓+3NH4+ |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,5.6L NO和5.6L O2混合后的分子总数为0.5NA |
| B.1mol Na2O2固体中含离子总数为4NA |
| C.7.1gCl2与足量NaOH溶液反应转移的电子数为0.2NA |
| D.在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA |