有A、B、C、D四种金属片,进行如下实验:①A、B用导线相连后,同时伸入稀H2SO4溶液中,A极为负极;②C、D用导线连接后浸入稀H2SO4中,电流由D 导线
导线 C;③A、C相连后同时浸入稀H2SO4中,C极产生大量气泡;④B、D相连后同时浸入稀H2SO4中,D极发生氧化反应,试判断四种金属的活动顺序是( )
C;③A、C相连后同时浸入稀H2SO4中,C极产生大量气泡;④B、D相连后同时浸入稀H2SO4中,D极发生氧化反应,试判断四种金属的活动顺序是( )
A.A>B>C>D B.A>C>D>B C.C>A>B>D D.B>D>C>A
有关电解质的下列叙述正确的是()
| A.离子化合物熔融状态时都导电,因此离子化合物都是电解质 |
| B.共价化合物熔融状态时都不导电,因此共价化合物都是非电解质 |
| C.易溶于水的化合物都是强电解质 |
| D.强电解质溶液的导电能力一定强 |
下列说法正确的是()
| A.水解反应是吸热反应 | B.升高温度可以抑制盐类的水解 |
| C.正盐水溶液pH均为7 | D.硫酸钠水溶液pH小于7 |
在AlCl3和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH的体积和所得沉淀的物质的量的关系如下图所示(b处NaOH溶液的体积为1L),则下列判断不正确的是 ( )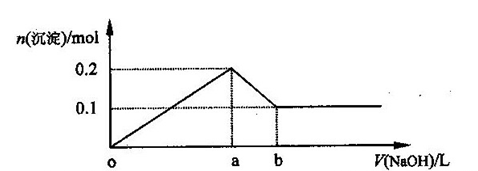
| A.NaOH的浓度为0.6 mol/L | B.在a点处溶液中的溶质为NaCl |
| C.在b点处溶液中的溶质只有NaAlO2 | D.图中线段oa : ab=5 : 1 |
下图是产生和收集气体的实验装置,该装置最适合于
| A.用浓硝酸与Cu反应制取NO2 |
| B.用浓盐酸和MnO2反应制取C12 |
| C.用NH4Cl和Ca(OH)2反应制取NH3 |
| D.用H2O2溶液和MnO2反应制取O2 |
以下物质间的每步转化通过一步反应能实现的是( )
| A.Al→Al2O3→Al(OH)3→NaAlO2 | B.Si→SiO2→H2SiO3→Na2SiO3 |
| C.S→SO3→H2SO4→MgSO4 | D.N2→NO→NO2→HNO3 |