1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,此反应的热化学方程式为( )
| A.C + H2O ==CO + H2ΔH ==+131.3KJ·mol—1 |
| B.C(s)+ H2O(g) ==CO(g) + H2(g)ΔH ==+10.94KJ·mol—1 |
C.C(s)+ H2O(l) ==CO(g) + H2(g)ΔH ==+ 131.3KJ·mol—1 131.3KJ·mol—1 |
| D.C(s)+ H2O(g) ==CO(g) + H2(g)ΔH ==+131.3KJ·mol—1- |
根据下列事实:①X+Y2+=X2++Y;②Z+2H2O(冷)=Z(OH)2+H2↑;③Z2+氧化性比X2+弱;④由Y、W电极组成的电池,电极反应为W2++2e-=W;Y-2e-=Y2+,可知X、Y、Z、W的还原性由强到弱的顺序为:
| A.X > Z > Y > W | B.Z > W > X > Y | C.Z > Y > X > W | D.Z > X > Y > W |
下列四种盐酸溶液,均能跟锌片反应,其中最初反应速率最快的是:
| A.10℃ 20mL 4mol/L的盐酸溶液 | B.20℃ 30mL 2mol/L的硫酸溶液 2mol/L的硫酸溶液 |
| C.20℃ 40mL 1mol/L的硫酸溶液 | D.20℃ 50mL 3mol/L的盐酸溶液 3mol/L的盐酸溶液 |
下列各组物质中,含有相同的化学键的是
| A.HI和NaI | B.H2S和CO2 | C.Cl2和KCl | D.F2和NaBr |
原子序数为z的元素R,在周期表中位于A、B、C、D四种元素的中间,A、B、C、D四种元素的原子序数之和为下列数据,其中不可能的是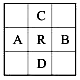
A.4z B.4z+10 C.4z+5 D.4z+14
在反应CaH2+2H2O=Ca(OH)2+2H2↑中,下列叙述正确的是
①H2是氧化产物②H2是还原产物③H2O是氧化剂④CaH2中氢元素既被氧化又被还原⑤生成1molH2时,电子转移1mol
| A.①②③④⑤ | B.①②③⑤ | C.④⑤ | D.①②③ |