下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
| A.Fe+CuSO4=FeSO4+Cu |
B.3CO+Fe2O3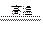 2Fe+3CO2 2Fe+3CO2 |
| C.AgNO3+NaCl=AgCl↓+NaNO3 |
D.2KMnO4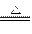 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
某无色透明溶液中存在大量的H+、Cl一、NO3一,该溶液中还可能大量存在的是
| A.HCO3一 | B.NH4+ | C.Cu2+ | D.Ag+ |
下列电离方程式错误的是
| A.CaCl2 =Ca2++2Cl- | B.Ba(OH)2=Ba2++2OH- |
| C.HNO3=H++NO3- | D.NaHCO3=Na++H++CO32- |
宋代著名法医学家宋慈的《洗冤集录》中有一“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2 =2Ag2S+2H2O。该反应中H2S是
| A.氧化剂 |
| B.还原剂 |
| C.既是氧化剂又是还原剂 |
| D.既不是氧化剂又不是还原剂 |
下列过程不涉及化学变化的是
| A.氢氟酸腐蚀玻璃 |
| B.过滤除去水中的泥沙 |
| C.食物变质腐烂 |
| D.烧菜用过的铁锅放置出现红棕色斑迹 |
有一种新型燃料电池,工作时在一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。现用该燃料电池和惰性电极电解Na2SO4溶液一段时间,假设电解时温度不变,下列说法不正确的是
| A.在熔融电解质中,O2-由正极移向负极 |
| B.电解一共生成0.9 mol气体时,理论上消耗0.1 mol丁烷 |
| C.电解池的阳极反应式为4OH--4e-===2H2O+O2↑ |
| D.通入空气的一极是正极,电极反应式为O2+4e-===2O2- |