常温下,用0.1000 mol·L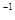 NaOH溶液滴定 20.00mL0.1000 mol·L
NaOH溶液滴定 20.00mL0.1000 mol·L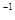
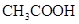 溶液所得滴定曲线如右图。
溶液所得滴定曲线如右图。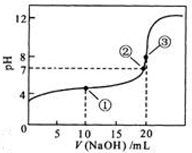
下列说法正确的是
A.点①所示溶液中: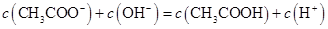 |
B.点②所示溶液中: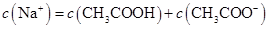 |
C.点③所示溶液中: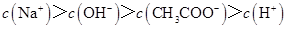 |
D.滴定过程中可能出现: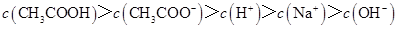 |
浓硫酸有许多重要的性质,在与含有水分的蔗糖作用过程中不能显示的性质是
| A.酸性 | B.脱水性 | C.强氧化性 | D.吸水性 |
能证明SO2具有漂白性的是
| A.酸性KMnO4溶液中通入SO2气体后溶液褪色 |
| B.滴入酚酞的NaOH溶液中通入SO2气体红色消失 |
| C.品红溶液中通入SO2气体红色消失 |
| D.溴水中通入SO2气体后溶液褪色 |
欲迅速除去铝壶底的水垢,最好的试剂是
| A.浓盐酸 | B.稀硝酸 | C.浓硫酸 | D.浓硝酸 |
下列物质的水溶液能导电,但属于非电解质的是
| A.H2SO4 | B.Cl2 | C.NaAlO2 | D.SO2 |
简单原子的原子结构可用下图的表示方法来形象表示,其中表示质子或电子,表示中子。则下列有关①②③的叙述中正确的是

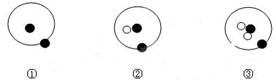
| A.①、②、③互为同位素 | B.①、②、③互为同素异形体 |
| C.①、②、③是三种化学性质不同的粒子 | D.①、②、③具有相同的质量数 |