据报道,科学家已成功合成了少量的O4,有关O4的说法正确的是
| A.O4的摩尔质量是64 g |
| B.O4与O2互为同位素 |
| C.相同质量的O4与O3所含原子个数之比为1∶1 |
| D.O4与O3、O2都是氧元素的同分异构体 |
据科学家预测,月球的土壤中吸附着数百万吨的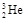 ,每百吨
,每百吨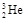 核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上氦元素主要以
核聚变所释放出的能量相当于目前人类一年消耗的能量。在地球上氦元素主要以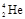 的形式存在。下列说法正确的是( )
的形式存在。下列说法正确的是( )
A.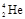 原子核内含有4个质子 原子核内含有4个质子 |
B.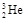 原子核内含有3个中子 原子核内含有3个中子 |
C.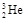 和 和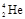 互为同位素 互为同位素 |
D.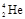 的最外层电子数为2,所以 的最外层电子数为2,所以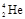 在反应中容易失去电子 在反应中容易失去电子 |
下列物质中属于强电解质的是()
| A.SO2 | B.Na2SO4 | C.Cl2 | D.CH3COOH |
今年入冬以年来我国多个城市出现大雾天气,致使高速公路关闭,航班停飞,雾属于下列哪种分散系
| A.乳浊液 | B.溶液 | C.悬浊液 | D.胶体 |
有一块铁的“氧化物”样品,用140mL 5.0mol·L-1 盐酸恰好将之完全溶解,所得溶液还能吸收0.025mol Cl2,恰好使其中的Fe2+全部转变为Fe3+,则该样品可能的化学式为( )
| A.Fe2O3 | B.Fe3O4 | C.Fe4O5 | D.Fe5O7 |
设NA代表阿伏加德罗常数的数值,下列说法正确的是
①常温常压下,17g甲基(-14CH3)所含的中子数为9NA;
②常温常压下,22.4LNO气体的分子数小于NA;
③64g铜发生氧化还原反应,失去2 NA个电子;
④常温常压下,100ml 0.5mol/l的乙酸溶液中,乙酸分子数目小于0.05NA;
⑤标况下,22.4LCCl4所含有的分子数为NA;
⑥常温常压下,1mol氦气含有的核外电子数为4 NA;
| A.②④ | B.①② | C.③④ | D.⑤⑥ |