(CN)2、(SCN)2、(OCN)2称“类卤素”,与卤素单质的性质相似,而其阴离子性质也相似,如:2Fe + 3(SCN)2 ="==" 2Fe(SCN)3,2Fe + 3Cl2 ="==" 2FeCl3。以此判断下列化学方程式中错误的是
A.(CN)2 + H2O HCN + HCNO HCN + HCNO |
B.(SCN)2 + 2Cu  2CuSCN 2CuSCN |
| C.(OCN)2 + 2NaOH ="==" NaOCN + NaOCNO + H2O |
D.MnO2 + 4HSCN(浓) (SCN)2 + Mn(SCN)2 + 2H2O (SCN)2 + Mn(SCN)2 + 2H2O |
在一定条件下,可逆反应:N2(g)+3H2(g)  2NH3(g),△H<0,达到平衡时,当单独改变下列条件后,有关叙述错误的是()
2NH3(g),△H<0,达到平衡时,当单独改变下列条件后,有关叙述错误的是()
| A.加催化剂V正、V逆都发生变化且变化的倍数相等 |
| B.加压,V正、V逆都增大,且V正增大倍数大于V逆增大倍数 |
| C.降温,V正、V逆都减小,且V正减小倍数小于V逆减小倍数 |
| D.加入氩气,V正、V逆都增大,且V正增大倍数大于V逆增大倍数 |
已知450℃时,反应H2(g)+I2(g) 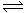 2HI(g)的K=50,由此推测在450℃时,反应
2HI(g)的K=50,由此推测在450℃时,反应
2HI(g) 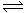 H2(g)+I2(g)的化学平衡常数为
H2(g)+I2(g)的化学平衡常数为
| A.50 | B.0.02 | C.100 | D.无法确定 |
体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2 2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
在一个固定体积的密闭容器中加入2 mol A和1 mol B发生反应2A(g)+B(g)  3C(g)+D(s),达到平衡时,混合气体中C的体积百分含量为a%,若维持容器的容积和温度不变,按下列四种配比方案作为反应物,达平衡后,C的体积百分含量不可能为a%的是()
3C(g)+D(s),达到平衡时,混合气体中C的体积百分含量为a%,若维持容器的容积和温度不变,按下列四种配比方案作为反应物,达平衡后,C的体积百分含量不可能为a%的是()
A.4 mol A+2 mol B |
B.3 mol C+1 mol D+2mol A+1 mol  B B |
| C.3 mol C+0.8 mol D | D.1.6 mol A+0.8 mol B+0.6 mol C+0.3 mol D |
某温度下的定容密闭容器中,进行如下可逆反应:A(s)+2B(g) C(g)+D(g),当下列物理量不发生变化时: ①混合气体的密度 ②容器内气体的压强 ③混合气体的平均相对分子质量 ④B的物质的量浓度能表明该反应一定已达到平衡状态的是 ()
C(g)+D(g),当下列物理量不发生变化时: ①混合气体的密度 ②容器内气体的压强 ③混合气体的平均相对分子质量 ④B的物质的量浓度能表明该反应一定已达到平衡状态的是 ()
| A.①③④ | B.②③ | C.②③④ | D.只有④ |