某学生想利用下图装置(烧瓶位置不能移动)收集下列气体:① H2 ②Cl2 ③CH4 ④HCl ⑤NH3 ⑥NO ⑦NO2 ⑧SO2,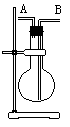
下列操作正确的是
| A.烧瓶是干燥的,由A进气收集①③⑤ |
| B.烧瓶是干燥的,由B进气收集②④⑥⑦⑧ |
| C.在烧瓶中充满水,由A进气收集①③⑤⑦ |
| D.在烧瓶中充满水,由B进气收集⑥ |
原电池电极的“正”与“负”不仅与电极材料的性质有关,也与电解质溶液有关.下列说法中正确的是( )
| A.由Fe、Cu和FeCl3溶液组成的原电池中,负极反应式为:Cu-2e-===Cu2+ |
| B.由Al、Cu和稀硫酸组成的原电池中,负极反应式为:Cu-2e-===Cu2+ |
| C.由Al、Mg和NaOH溶液组成的原电池中,负极反应式为:Al+4OH--3e-===AlO+2H2O |
| D.由Al、Cu和浓HNO3溶液组成的原电池中,负极反应式为:Al-3e-===Al3+ |
强酸与强碱的稀溶液发生中和反应的热化学方程式为:
H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3kJ/mol,分别向1 L 0.5mol/L的NaOH溶液中加入:①稀醋酸;②浓H2SO4;③稀硝酸。恰好完全反应时的热效应分别为ΔH1、ΔH2、ΔH3,它们的关系正确的是( )
| A.ΔH1>ΔH2>ΔH3 |
| B.ΔH2>ΔH3>ΔH1 |
| C.ΔH1=ΔH2=ΔH3 |
| D.ΔH1>ΔH3>ΔH2 |
铜锌原电池(如下图)工作时,下列叙述正确的是 ()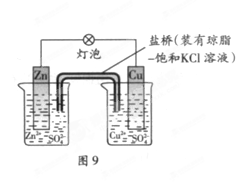
| A.正极反应为:Zn—2e-=Zn2+ |
| B.电池反应为:Zn+Cu2+=Zn2+ +Cu |
| C.在外电路中,电子从正极流向负极 |
| D.盐桥中的K+移向ZnSO4溶液 |
已知反应A2+B2===2AB,破坏1 mol A2中的化学键消耗的能量为Q1 kJ,破坏1 mol B2中的化学键消耗的能量为Q2 kJ,形成1 mol AB中的化学键释放的能量为Q3 kJ,则下列说法正确的是( )
| A.若该反应为吸热反应,则Q1+Q2<2Q3 |
| B.若该反应为放热反应,则Q1+Q2>Q3 |
| C.若A2和B2的总能量之和小于生成的AB的总能量,则反应放热 |
| D.若A2和B2的总能量之和大于生成的AB的总能量,则反应放热 |
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如右下图所示。常温下,S2Cl2遇水易发生反应,并产生能使品红褪色的气体。下列说法错误的是()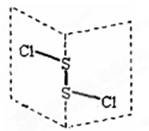
A.S2Cl2的电子式为 |
| B.S2Cl2同时含有极性键和非极性键 |
| C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2 > S2Cl2 |
| D.S2Cl2与H2O反应的化学方程式可能为: |
2S2Cl2+2H2O = SO2↑+3S↓+4HCl