酒精又称为乙醇,除可以用于制作含醇饮料外也是一种清洁燃料。用淀粉酿制乙醇的化学反应方程式是:
↑
[注:
的相对分子质量是
]。计算(结果保留1位小数):
(1)
的相对分子质量是
(2)
淀粉理论上可以制得乙醇的质量是多少?
(3)假设醉酒驾车的标准是人体血液中乙醇含量超过
。若人体中血液占人体体重的10%(假设血液的密度是:
),则:

①.一个体重为
的驾驶员血液中所含乙醇的总质量不能超过多少?
②.①中结果相当于质量分数为50%的白酒的质量是多少?
如图是实验室制取气体的常用装置,请回答下列问题:

(1)写出图中标号仪器的名称:① ② 。
(2)实验室可用过氧化氢溶液与MnO2制取O2,该反应中MnO2是 ,请写出该反应的化学方程式: 。若用E装置收集O2,当 时,开始收集。
(3)实验室可用Zn粒与稀硫酸制取H2.应选用的气体发生装置是 (填字母),该装置优点为 。若要收集干燥的H2,应将生成的H2依次通过F、D装置,F装置中盛放的液体是 (填名称),选择D装置收集H2的原因是 (填H2的物理性质)。
NaOH俗称火碱、烧碱、苛性钠,是常见的碱,请回答下列问题:
(1)NaOH的名称是 ,易溶于水,溶于水生成自由移动的 (填微粒符号),所以NaOH溶液能够导电。
(2)向NaOH溶液中滴加稀硫酸,溶液的pH (填”增大”、“减小”或“不变”)。
(3)在试管中加入2mL 10%NaOH溶液,滴加5%CuSO4溶液4﹣5滴,生成 色的Cu(OH)2沉淀。用试管中的物质检验葡萄糖,发生如下反应:C6H12O6+2Cu(OH)2+NaOH C6H11O7Na+Cu2O↓+3X,推测X的化学式为 。
(4)参考如图,在( )内画出“→”或“﹣”补全图例(“→”表示物质间转化,“﹣”表示物质间相互反应)。请写出图例中,能发生复分解反应的化学方程式: (写出一个即可)。

氢气与氧气在一定条件下可以发生化学反应。根据所给信息,请回答下列问题:

(1)纯净的氢气在空气中燃烧时产生淡蓝色火焰、放出热量、烧杯内壁凝结有 ,写出发生反应的化学方程式 。
(2)化学变化是反应物的 重新组合转变成生成物的过程。从氧气变为水时,氧元素化合价的具体变化是 。
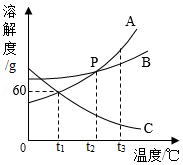
如图是A、B、C三种固体物质的溶解度曲线。
(1)P点表示的含义是 。
(2)t1℃时,将35gA物质加入到50g水中,形成 (填“饱和”或“不饱和”)溶液。
(3)B中混有少量的A,提纯B的方法是 。
(4)将等质量的A、B、C三种固体物质分别配成t3℃时的饱和溶液,所得溶液的质量最多的是 。
(5)将t1℃时A、B、C三种物质的饱和溶液升温到t3℃时,所得溶液的溶质质量分数由大到小的关系是 。
如图是某化学反应的微观示意图,请根据图示回答下列问题。
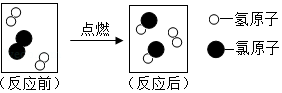
(1)参加反应的反应物的粒子个数比为 ;
(2)该化学变化中不发生改变的粒子是 (填“分子”或“原子”)。
(3)一个“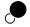 ”分子是由 个原子构成的。
”分子是由 个原子构成的。
(4)该反应的化学方程式为 。