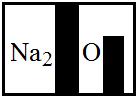在查阅资料时,小明得知
在高温条件下能与木炭反应生成
。他决定对该反应进行探究。
[提出问题]
与木炭在高温条件下反应是否生成
?
[实验探究]小胡设计了如图的实验方案,并进行实验。

(1)
中用石灰石与稀盐酸反应生成
,反应的化学方程式为。
(2)
中装有饱和碳酸氢钠溶液,其作用是除去
气体中混有的少量
气体。
中装有浓硫酸。其作用是。
(3)
中装入氢氧化钠溶液的作用是。
[实验结论]经检验
处的气体为
。结论:
在高温条件下与木炭反应生成了
。
[实验反思] (4)有同学对
装置作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中。改进后的优点是。
[实验拓展] (5)撤去
,按
顺序连接。然后
中用二氧化锰和过氧化氢溶液混合生成
,反应的化学方程式为。此时要检验该实验条件下
中木炭所发生反应的生成物,还需要补充和完善的实验是。
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。
探究一:该气体的成分。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_________________________________________________________。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO___________________________________________________。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
| 实验编号 |
实验操作 |
实验现象 |
| ① |
将气体通入澄清的石灰水中 |
澄清石灰水变浑浊 |
| ② |
将带火星的木条伸入该气体中 |
带火星的木条没有复燃 |
【得出结论】(1)由实验①可知,该气体中肯定含有_________,写出该反应的化学方程式_____________________________________________________。
(2)由实验②_____________(填“能”或“不能”)确定该气体中不含氧气,理由是_________________________________________________________________________________。
已知,过氧化钠(化学式为Na2O2)是一种浅黄色固体粉末,可用作呼吸面具里的供氧剂利用人呼出的二氧化碳与过氧化钠反应放出氧气,供给人的正常生命活动,该反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2。某同学利用该反应原理制取氧气,设计实验装置如下图所示:
(1)装置①中CO2的制取方法有多种:若用稀盐酸和石灰石制取CO2,该反应的化学方程式为。若用加热NaHCO3固体制取CO2,应该选用的发生装置为(选填下图字母)
(2)④为O2的收集装置,可选用装置 (选填上图字母)。
某研究小组欲检验草酸晶体样品分解产物,并测定样品中草酸晶体的质量分数(假设杂质不参与反应)。已知:浓硫酸可作为干燥剂;草酸晶体(H2C2O4·2H2O )的性质见下表:
| 熔点 |
沸点 |
热稳定性 |
其他 |
| 101℃~102℃ |
150℃~160℃升华 |
100.1℃分解出水,175℃分解成CO2、CO、H2O |
与 Ca(OH)2反应产生白色沉淀(CaC2O4) |
(1)图 1 是加热装置。最适宜的加热分解草酸晶体装置是C。若选装置 a 可能会造成的后果是_____________________;若选装置B可能会造成的后果是_________________。
(2)图 2 是验证热分解产物中含 CO 、 CO2的装置。
① 装置 A 的作用是_____________________,气囊的作用是_____________________。
② 证明存在 CO2的现象是______________,证明存在 CO 的现象是______________。
(3)为测定样品中草酸晶体的质量分数,设计如下方案:称取一定量样品,用上述装置进行实验,称量装置D反应前后的质量差。由此计算出的实验结果比实际值偏低,排除仪器和操作因素,其可能原因:_________________________________________________。
同学们为了研究氧化铁能否在氯酸钾制取氧气的实验中起催化作用,进行了以下实验:
【资料】①氯酸钾分解反应的化学方程式为 2KClO3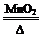 2KCl+3O2↑。
2KCl+3O2↑。
②氯酸钾和氯化钾均能溶于水。
【实验一】氧化铁能否在氯酸钾制取氧气实验中加快反应速率。
| 实验编号 |
KClO3/g |
氧化物 |
产生气体的体积(mL) |
耗时(s) |
| 1 |
0.6 |
67 |
1800 |
|
| 2 |
0.6 |
0.2g二氧化锰 |
67 |
36.5 |
| 3 |
0.6 |
g 氧化铁 |
67 |
89.5 |
(1)实验3中氧化铁的质量为。
(2)以上实验采用了的实验方法。
(3)实验一得到的结论是。
【实验二】为证明氧化铁是该反应的催化剂,同学们又完成了以下的实验:
Ⅰ.在实验3反应后的混合物中加足量的水溶解,过滤得到红色固体,洗涤干燥并用电子天平称量,质量为0.2g。
Ⅱ.将一定量的CO通入滤出的固体,按下图进行实验: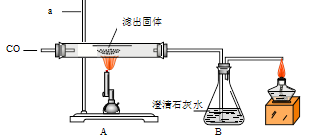
甲同学的实验报告如下:
| 装置 |
实验现象 |
实验分析 |
| A |
红色固体全部变黑 |
生成了铁 |
| B |
石灰水变浑浊 |
产生二氧化碳 |
(4)写出A中玻璃管内发生反应的化学方程式。
【实验结论】氧化铁能在氯酸钾制取氧气反应中起催化剂。
【实验反思】乙同学查阅资料发现一氧化碳还原氧化铁后剩余固体可能由氧化亚铁、四氧化三铁、铁粉和未反应的氧化铁中的一种或几种组成。
为了研究剩余固体的成分,丙同学查阅了以下资料:
| 铁粉 |
氧化亚铁 |
氧化铁 |
四氧化三铁 |
|
| 颜色 |
黑色 |
黑色 |
红色 |
黑色 |
| 磁性 |
有 |
无 |
无 |
有 |
| 与CO反应 |
不反应 |
反应 |
反应 |
反应 |
| 与稀盐酸反应 |
反应 |
生成氯化亚铁和水 |
生成氯化铁和水 |
生成氯化亚铁、氯化铁和水 |
| 与硫酸铜溶液反应 |
反应 |
不反应 |
不反应 |
不反应 |
(5)丙同学认为剩余固体中一定没有氧化铁,原因是____________。
(6)测定剩余固体的组成。
| 步骤 |
实验操作 |
实验现象 |
结论和解释 |
| 1 |
用磁铁吸引剩余固体 |
_____________ |
剩余固体中没有氧化亚铁。 |
| 2 |
__________________ |
______________ |
剩余固体中只有铁粉。 |
酸、碱、盐是几类有广泛用途的重要化合物.
(1)酸和碱在组成和性质方面有很多共同的特点,请任写出其中的一条.
(2)氢氧化钙是一种常见的碱,列举其在生产、生活中的一种用途.
(3)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如右图)的溶液,他们对此产生了兴趣.
提出问题:这瓶溶液究竟是什么?
经过询问实验老师平时的药品保管得知,这瓶无色溶液应该是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中的某一种.为了确定该药品,他们首先进行了理论分析:
①小明根据标签上的组成元素认为一定不可能是 (提示:只有其中一种).
②小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是:
设计实验:为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验.
| 实验操作 |
实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液 |
出现白色沉淀 |
| 静置一段时间后,倾去上层清液,向沉淀中滴加稀盐酸 |
白色沉淀全部溶解,并产生大量气泡 |
实验结论:③该瓶无色溶液是 .出现白色沉淀过程的化学方程式是: .
实验反思:④小强认为上述设计实验还可简化,也能达到目的.小强的实验操作是:
(4)若73 g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数.