下列各组离子能在强酸性溶液中大量共存的是
| A.K+、Na+、CO32-、SO3 2- | B.Mg2+、Na+、Cl—、SO42- |
| C.Ba2+、Na+、CO32-、 OH- | D.Ag+、K+、Cl—、NO3- |
下列说法正确的是
| A.熔化干冰和熔化NaCl晶体所克服的作用力相同 |
| B.氢键比分子间作用力强,所以它属于化学键 |
| C.H2O是一种非常稳定的化合物,这是由于氢键所致 |
| D.冰的密度比水小,这是由于冰中存在氢键所致 |
硝酸被称为“国防工业之母”是因为它是制取炸药的重要原料。下列实验事实与硝酸性质不相对应的一组是 ( )
| A.浓硝酸使紫色石蕊试液先变红后褪色——酸性和强氧化性 |
| B.不能用稀硝酸与锌反应制氢气——强氧化性 |
| C.要用棕色瓶盛装浓硝酸——不稳定性 |
| D.稀硝酸能使滴有酚酞的氢氧化钠溶液红色褪去——强氧化性 |
短周期金属元素A~E在元素周期表中的相对位置如表所示,下面判断正确的是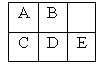
| A.原子半径:C<D<E |
| B.金属性:A>C |
| C.氢氧化物的化学式及其碱性:COH>D(OH)2>E(OH)3 |
| D.最外层电子数:A>B |
A元素原子最外层电子数是次外层电子数的3倍,B元素原子次外层是最外层电子数的2倍,则关于A、B元素的判断正确的
A. A和B元素不一定都是短周期元素 B. A和B元素一定是同一主族元素
C.A和B元素一定都是非金属元素 D. A、B可以相互化合形成化合物BA2或B2A
下列说法正确的是
①元素原子的最外层电子数等于元素的最高化合价
②最外层一个电子的元素一定是金属元素,肯定在元素周期表的第IA族
③所有元素的原子最外层最多可容纳的电子数均为8
④第三周期元素随原子序数增大各非金属元素对应的氧化物的水化物酸性一定逐渐增强
⑤同主族元素随原子序数增大,其原子半径逐渐增大
| A.①②③④⑤ | B.①②③ | C.④⑤ | D.⑤ |