下列实验操作中错误的是
| A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C.可用酒精萃取碘水中的碘 |
| D.称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘 |
在一定温度下,一定量的水中,石灰乳悬浊液存在下列平衡:
Ca(OH)2(s) 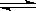 Ca2+(aq) + 20H-(aq),当向此悬浊液中加入少量氧化钙固体时,下列说法正确的是
Ca2+(aq) + 20H-(aq),当向此悬浊液中加入少量氧化钙固体时,下列说法正确的是
| A.c(Ca2+)增大 | B.c(Ca2+)不变 |
| C.c(OH-)增大 | D.Ca(OH)2固体的质量不变 |
下列措施能加快Fe与0.1mol/L的稀H2SO4反应产生H2的反应速率的是
| A.向溶液中再滴加1mol/L的HNO3 | B.将稀硫酸改为98%的浓硫酸 |
| C.滴加少量的CuSO4溶液 | D.降低温度 |
在一定温度下的恒容容器中,当下列物理量不再发生变化时,表明反应A(s)+3B(g)  2C(g)+D(g)已达平衡状态的是
2C(g)+D(g)已达平衡状态的是
A.混合气体的压强B.混合气体的总物质的量
C.气体的平均分子量D.v(B)=3V(D)
关于氯化铁水解的错误说法是
| A.水解达到平衡(不饱和)时,无论加氯化铁饱和溶液还是加水稀释,平衡均向正方向移动 |
| B.浓度为5mol/L和0.5mol/L的两种FeCl3溶液,其它条件相同时,Fe3+的水解程度前者比后者低 |
| C.有50℃和20℃的相同浓度氯化铁溶液,其他条件相同时,Fe3+的水解程度前者比后者小 |
| D.为抑制Fe3+水解,较好地保存FeCl3溶液,应加少量盐酸 |
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见下图,电池总反应可表示为:2H2+O2===2H2O,下列有关说法正确的是
| A.电子通过外电路从b极流向a极 |
| B.b极上的电极反应式为O2+2H2O+4e-===4OH- |
| C.每转移0.2 mol电子,消耗标准状况下1.12 L的H2 |
| D.H+由a极通过固体酸电解质传递到b极 |