在气相条件下(T="500" K),有相同体积的甲、乙两容器,甲容器充入1 g SO2、l gO2,乙容器充入2 g SO2、2g O2则下列叙述中正确的是
| A.化学反应速率:乙>甲 | B.平衡后SO2的浓度:乙>甲 |
| C.SO2转化率:乙<甲 | D.平衡后O2的体积分数:乙>甲 |
已知:2Zn(s)+O2(g)=2ZnO(s) △H=-701.0kJ·mol-1
Hg(l)+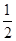 O2(g)=HgO(s) △H=-90.8kJ·mol-1
O2(g)=HgO(s) △H=-90.8kJ·mol-1
则反应Zn(s)+ HgO(s)=ZnO(s)+ Hg(l)的△H为
| A.-259.7 kJ·mol-1 | B.+259.7 kJ·mol-1 |
| C.+519.4kJ·mol-1 | D.-519.4kJ·mol-1 |
对于铁在海水的腐蚀及防护设计实验如下(烧杯中装的是海水),以下描述正确的是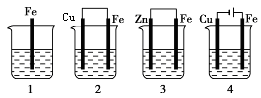
| A.1中的铁被腐蚀得最快 |
| B.2中的铁被腐蚀得最慢 |
| C.3中是电化学防腐蚀的运用,称为牺牲阳极的阴极保护法 |
| D.4中装置也能起到防止铁被腐蚀的作用 |
设NA是阿伏伽德罗常数的数值,下列说法正确的是
| A.1molNa+离子含有的核外电子数为NA |
| B.1molCl2与足量的铁反应,转移的电子数为3NA |
| C.标准状况下,22.4L的CCl4中含有的CCl4分子数为NA |
| D.常温下,10LpH=13的NaOH溶液中含有的OH-离子数为NA |
短周期元素W、X、Y、Z在元素周期表中的位置如右图所示。下列说法中,正确的是
| X |
||
| Y |
||
| Z |
W |
A.Y的原子半径在同周期主族元素中最大
B.W的最高价氧化物对应的水化物是强酸
C.X原子最外层电子数为8
D.Z的气态氢化物的稳定性在同主族元素中最强
能正确表示下列反应的离子方程式是
| A.少量Cl2通入KI溶液中:Cl2+ 2I- =2C1- + I2 |
| B.碳酸钙溶于稀硝酸中:CO2- 3 + 2H+ =H2O + CO2↑ |
| C.醋酸钠水溶液中通入足量CO2:2CH3COO- + CO2 + H2O = 2CH3COOH + CO2- 3 |
| D.金属铝溶于稀硫酸中:Al + 2H+ = A13+ + H2↑ |