A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的气球.
关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应开始时,A、B的体积相同。已知:2NO2(g) N2O4(g)△H<0。
N2O4(g)△H<0。
(1)一段时间后,反应达到平衡,此时A、B中生成的N2O4的速率是V(A) V(B)(填“<”、“>”或“=”);若打开活塞K2,气球B将 (填“变大”、“变小”或“不变”,下同)。
(2)若在A、B中再充入与初始量相等的NO2,则达到平衡时,NO2的转化率α(A)将 。
若通入等量的Ne气,则达到平衡时,A中NO2的转化率将 ,B中NO2的转化率将 。
(3)室温时,若A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时, 中的颜色较深。
(4)若在容器A中充入4.6g的NO2,达到平衡后容器内混合气体的压强为原来的80%,试求出平衡时NO2的转化率(写出计算过程)
在氧化还原反应3S+6KOH===K2SO3+2K2S+3H2O中,被氧化与被还原的硫原子数之比为()
| A.1:2 | B.2:1 | C.1:1 | D.3:2 |
下列溶液中能够区别SO2和CO2气体的是()
①石灰水②H2S溶液③KMnO4溶液④氯水⑤品红溶液
| A.①②③ | B.②③④ | C.除①以外 | D.全部 |
在四种化合物①NaHCO3②Al(OH)3③Al2O3④Al2(SO4)3中跟盐酸和氢氧化钠溶液都能反应的是()
| A.只有②④ | B.只有①② | C.只有①②③ | D.①②③④ |
下列物质与常用危险化学品的类别不对应的是()
| A.H2SO4、NaOH——腐蚀品 | B.SO2、NO2——易燃液体 |
| C.Na——遇湿易燃物品 | D.KMnO4、K2Cr2O7——氧化剂 |
NA代表阿伏加德罗常数,下列判断正确的是()
A.2.4g金属Mg变为Mg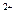 时失去的电子数为0.1 NA 时失去的电子数为0.1 NA |
| B.等物质的量的N2和CO所含原子数相同,质量相同 |
| C.在标况下,22.4 L H2O所含氢原子为2NA |
D.1L 0.1 mol·L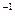 的乙酸溶液中H 的乙酸溶液中H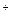 数为0.1 NA 数为0.1 NA |