X、Z、Q、R 4种短周期元素原子序数的依次增大,Y是一种短周期主族非金属元素。化合物甲由X、Z、Q 3种元素组成,常温下,0.1mol·L-1甲溶液的pH=13。工业上常用电解QR饱和溶液生产甲。请填写下列空白。
(1)Q的原子结构示意图为 。
(2)电解QR饱和溶液反应的离子方程式为 。
(3)常温下将R的单质通入甲溶液中,发生反应的离子方程式为 。
(4)①若Y与X组成的气体化合物乙在常温下遇XR气体时产生白烟,则乙的化学式为 ;YZ2与水反应的化学方程式:________________________________________
②若Y元素的单质能发生如图所示转化,则Y元素名称是 。YZ2的结构式为:_____________YZ2通过置换反应可生成Y的单质,该反应式为:____________________________________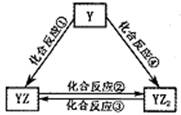
③若Y元素的单质是一种淡黄色固体。写出Y的最高价氧化物的水化物的浓溶液与铜共热的化学方程式:______________ ____________________________________
④若Y的最高价氧化物可制光导纤维。写出工业生产Y单质的反应的化学方程式:____________________________________________________________
有机物A(分子式C6H10O3)是合成某种隐形眼镜材料的单体,A可发生如下变化:
已知:Ⅰ.物质B是最简单的二元醇,可用作汽车发动机抗冻剂;物质D不能发生银镜反应,但能与NaHCO3溶液反应放出气体。
Ⅱ.
回答下列问题:
(1)隐形眼镜材料的结构简式为;
(2)写出物质B在铜催化下与O2反应的化学方程式;
(3)与C互为同分异构体,分子为链状的酯类物质共有种;
(4)请设计合理方案,用物质D制取乙二酸(其他无机原料自选,用反应流程图表示,并注明必要的反应条件)。
例如:
将a mol的Na2O2和b mol NaHCO3固体混合后,在密闭容器中加热到250℃,让其充分反应,假设NaHCO3分解产生的CO2与Na2O2反应完后,H2O再与Na2O2反应.
(1)当剩余固体为Na2CO3,排出气体为O2,H2O时,a与b的比值为________.
(2)当剩余固体为Na2CO3,NaOH,排出气体为O2,H2O时,a与b的比值为________.
(3)当a大于b时,剩余固体为________,排出气体为________.
(4)排出的O2和H2O为等物质的量时,则a与b的比值为________.
(11)下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。
根据图示回答问题:
(1)写出下列物质的化学式:A_________,E_________ ,I_____________;
(2)反应①的化学方程式是______________________________;
反应②的化学方程式是_______________________;
(3)J与盐酸反应的化学方程式是__________________________;
反应后的溶液与D反应的化学方程式是__________________________________。
(8分)根据下式所示的氧化还原反应设计一个原电池:Cu + 2Ag+ =Cu2+ + 2Ag
(1)装置可采用烧杯和盐桥,画出此原电池的装置简图;
(2)注明原电池的正极和负极,以及外电路中电子流向;
(3)写出两个电极上的电极反应式;
钢铁容易生锈的主要原因是因为钢铁在炼制过程中混有少量的碳杂质,在潮湿的空气中容易形成原电池,发生电化学腐蚀。在空气酸度不大的环境中,其负极是,负极反应式为;正极是,正极反应式为。