向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)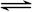 SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如下所示。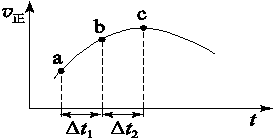
图6
由图可得出的正确结论是( )
| A.反应在c点达到平衡状态 |
| B.反应物浓度:a点小于b点 |
| C.反应物的总能量低于生成物的总能量 |
| D.Δt1=Δt2时,SO2的转化率:a~b段小于b~c段 |
利用如下图所示装置,当X、Y选用不同材料时,可将电解原理广泛用于工业生产。下列说法中正确的是
| A.氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠 |
| B.铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 |
| C.电镀工业中,X是待镀金属,Y是镀层金属 |
| D.外加电流的阴极保护法中,Y是待保护金属 |
列四个图象的说法中正确的是
| A.图①表示将SO2气体通入溴水中溶液的pH随SO2气体变化关系 |
B.图②表示反应N2(g)+3H2(g) 2NH3(g),△H<0的平衡常数K随温度的变化 2NH3(g),△H<0的平衡常数K随温度的变化 |
| C.图③中阴、阳两极收集到的气体体积之比一定为1:1 |
| D.图④中的△H1<△H2 |
下列有关说法,不正确的是
①形成化学键的过程一定是化学变化②铁分别与氯气和稀盐酸反应所得的氯化物相同 ③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化④常温下,pH=12的溶液一定能大量存在:K+、Cl-、SO32-、S2在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是:范德华力、共价键、共价键
| A.①②③⑤ | B.②③④ | C.①③④ | D.①②④⑤ |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,11.2LSO3所含的分子数为0.5NA |
| B.12g石墨和C60的混合物中质子总数一定为6NA |
| C.25℃时,1L mol•L-1FeCl3溶液中含有0.1NA个Fe(OH)3胶体粒子 |
| D.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA |
下列说法正确的是
| A.Mg、Al在空气中性质稳定,因而都具有很强的抗腐蚀性 |
| B.质量数相等的不同核素,一定属于不同种元素 |
| C.生石灰、铁粉、硅胶是食品包装中常用的干燥剂 |
| D.自行车钢架生锈主要是化学腐蚀所致 |