如图为铜锌原电池示意图,下列说法中正确的是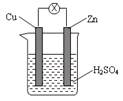
| A.锌片逐渐溶解 |
| B.烧杯中溶液逐渐呈蓝色 |
| C.电子由铜片通过导线流向锌片 |
| D.该装置能够将电能转化为化学能 |
下列离子方程式改写成化学方程式正确的是
| A.Cu2+ +2OH- =Cu(OH)2↓ CuCO3+2NaOH=Cu(OH)2↓+Na2CO3 |
| B.CO32- + 2H+ = CO2 ↑+ H2OBaCO3 + 2HCl =BaCl2+ CO2↑ + H2O |
| C.Ca2+ + CO32- = CaCO3↓Ca(NO3)2+NaCO3 = CaCO3↓+NaNO3 |
| D.H+ +OH- = H2OBa(OH)2+2HNO3 = Ba(NO3)2 +2H2O |
一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则生成1 mol Cr2O72-反应所需PbO2的物质的量为
| A.3.0 mol | B.1.5 mol | C.1.0 mol | D.0.75 mol |
黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成的,爆炸时的反应是:
S+2KNO3+3C = K2S+N2↑+3CO2↑,该反应的还原剂是
| A.C | B.C和S | C.KNO3 | D.S和KNO3 |
下列各组离子一定能大量共存的是
| A.在无色溶液中:NH4+、Fe2+、SO42-、CO32- |
| B.在含大量Ba2+的溶液中:Cu2+、Na+、Cl-、OH- |
| C.在强酸性溶液中:K+、Fe2+、Cl-、CH3COO- |
| D.在强碱溶液中:Na+、K+、Cl-、SO32- |
除去下列物质中的少量杂质(括号内的物质为杂质),加入试剂或方法不正确的是
| A.NaCl溶液(BaCl2):加入足量Na2CO3溶液,过滤,再向滤液中加适量盐酸并加热 |
| B.KNO3溶液(AgNO3):加入足量KCl溶液,过滤 |
| C.NaCl固体(Na2CO3):加适量稀盐酸,加热蒸发 |
| D.CO2(HCl):将混合气体通过NaHCO3饱和溶液 |