下列各组离子在指定溶液中一定能大量共存的是:
| A.强碱性溶液中:Ca2+、K +、HCO3—、Cl— |
| B.酸性的溶液中:Fe2+、NO3—、Na+、SO32— |
| C.使红色石蕊试液变蓝的溶液中:NH4+、Mg2+、K +、SO42— |
| D.加入镁条能放出氢气的溶液中:Fe3+、Cl—、SO42—、Na+ |
某烯烃与H2加成后得到2,2 二甲基丁烷,该烯烃的名称是()
二甲基丁烷,该烯烃的名称是()
A.2,2 二甲基 二甲基 3 3 丁烯 丁烯 |
B.2,2 二甲基 二甲基 2 2 丁烯 丁烯 |
C.2,2  二甲基 二甲基 1 1 丁烯 丁烯 |
D.3,3 二甲基 二甲基 1 1 丁烯 丁烯 |
下列说法中正确的是()
A.按系统命名法,有机物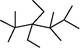 的命名为2,3,3,5,5 的命名为2,3,3,5,5 五甲基4,4二乙基己烷 五甲基4,4二乙基己烷 |
| B.已知C—C键可以绕键轴自由旋转,甲苯分子中最多有13个原子处于同一平面上 |
| C.用溴水可以除去苯中混有的苯酚 |
| D.菜籽油、牛油、甘油等都属于酯,均能与氢氧化钠溶液发生皂化反应 |
关于苯乙烯( )的下列叙述中,正确的是()
)的下列叙述中,正确的是()
| A.分子中所有原子一定在同一平面内 |
| B.不能使KMnO4酸性溶液褪色 |
| C.不能使溴的CCl4溶液褪色 |
| D.可通过加聚反应生成高分子化合物 |
2016年夏季奥运会将在“足球王国”——巴西首都里约热内卢举行,下图酷似奥林匹克旗中的五环的一种有机物被称为奥林匹克烃,下列说法中正确的是()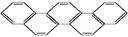
| A.该有机物属于芳香族化合物,是苯的同系物 |
| B.该有机物是只含非极性键的非极性分子 |
| C.该有机物的一氯代物只有一种 |
| D.该有机物完全燃烧生成H2O的物质的量小于CO2的物质的量 |
下列叙述中正确的是()
A.(CH3)2C CHCH2CH3中所有碳原子共面 CHCH2CH3中所有碳原子共面 |
| B.苯不能使酸性高锰酸钾溶液褪色,证明苯分子中不存在单双键交替的结构 |
| C.聚乙烯能使溴水褪色 |
| D.甲醇、乙二醇(HOCH2CH2OH)互为同系物 |