汽车尾气里含有NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:
N2(g) + O2(g)  2NO(g) △H > 0
2NO(g) △H > 0
已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
(1)该反应的平衡常数表达式为 。
(2)该温度下,向2L密闭 容器中充入N2和O2各1mol,平衡时,N2的转化率是 %
容器中充入N2和O2各1mol,平衡时,N2的转化率是 %
(保留整数)。
(3)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L
和3.0×10-3mol/L,此时反应 (填“处于化学平衡状态”、“向
正反应方向进行”或“向逆反应方向进行”),理由是
(4)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是 (填字母序号)。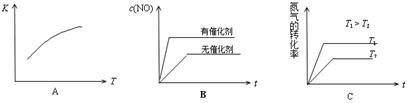
(5)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入
一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的
体积分数 (填“变大、“变小”或“不变”)。
甲醇是可再生燃料,可以利用天然气等物质生产,生产成本低,用途广泛。最近有科学家提出:把含有0.050%CO2的空气(通常情况下空气中CO2的体积分数为0.030%,当空气中CO2的体积分数超过0.050%时,会引起明显的温室效应。)吹入碳酸钾溶液中,然后再想法把CO2从溶液中提取出来,经化学反应后得到甲醇,其构想技术流程如下:
试回答下列问题:
(1)写出吸收池中主要反应的离子方程式:
_______________________。
(2)写出合成塔中反应的化学方程式:
____________________。
(3)若吹入的空气体积为33.6m3(标准状况下),则理论上最多可生产g甲醇
在如下图用石墨作电极的电解池中,放入500mL硫酸铜溶液进行电解,当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g。请回答下列问题:
(1)A接的是电源的极,B是该装置的 极。
(2)写出电解时B极的电极反应式式
(3)写出电解时反应的总离子 方程式
方程式 。
。
若电解后溶液的体积仍为500mL,该溶液的PH为
短周期元素X、Y、Z在元素周期表中的位置如右图所示,它们的质子数之和为21。
(1)氢元素与Z形成原子个数比为1∶1的化合物,其电子式为_____________。该化合物分子中存在__________(填“共价键”或“离子键”)。
(2)Y最高价氧化物的水化物与Y的氢化物恰好完全反应时,生成物的 水溶液呈酸性,其原因是_________________________________________;(用离子方程式表示)
水溶液呈酸性,其原因是_________________________________________;(用离子方程式表示)
该溶液中各种离子浓度由大到小顺序为______________________________。
(3)①恒温下,在容积为2L的刚性容器中充入2mol H2与2mol Y的单质,5分钟后反应达到平衡时,此时Y的单质为1.8mol,则产物的反应速率为
平衡时容器内压强与反应前压强比为__________;
②若该反应在恒温恒压条件下进行(其它条件相同),反应达到平衡时,H2的转化率比上述条件下H2的转化率_______(填“大”、“小”或“相同”)。
(4)常温下,由X的最简单气态氢化物3.2g在氧气中完全燃烧后恢复至常温 ,放出a kJ 的热量,试写出该反应的热化学方程式:____________________________________。
,放出a kJ 的热量,试写出该反应的热化学方程式:____________________________________。
A、B、C、D均为中学化学常见的物质。它们之间存在如下图所示的转化关系时。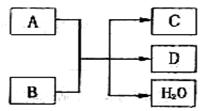
(1)若A为Cl2,B为Ca(OH)2,常温下反应的化学方程式为:
______________________________________
该反应的还原剂是
若有1molCl2参加反应,则反应中转移的电子数为
(2)若A为单质,C、D均为能使澄清石灰水变浑浊的无色气体,B的化学式为。
在常温下,有下列九种物质:
①石墨 H2S③CaCO3④液态NH3
⑤CH3COONH4 晶体⑥CO2⑦Na Cl溶液⑧Na
⑨CH3CH2OH
请根 据要求填写下列空白:(填序号)
据要求填写下列空白:(填序号)
(1)属于非电解质的是;
(2)属于强电解质的 是;
是;
(3)在上述九种物质中,能导电的是;
(4)写出下列物质的电离方程式:H2S