“碳捕捉技术”是指通过一定的方法将工业生产中产生的CO2分离出来并利用。如可利用NaOH溶液来“捕捉”CO2,其基本过程如下图所示(部分条件及物质未标出)。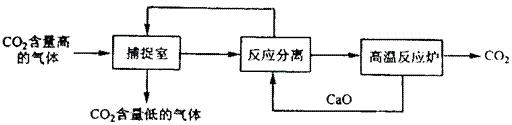
下列有关该方法的叙述中正确的是( )
| A.能耗大是该方法的一大缺点 |
| B.整个过程中,只有一种物质可以循环利用 |
| C.“反应分离”环节中,分离物质的基本操作是蒸发结晶、过滤 |
| D.该方法可减少碳排放,捕捉到的CO2还可用来制备甲醇等产品 |
下面的排序错误的是()
| A.硬度由大到小:金刚石>碳化硅>晶体硅 |
| B.熔点由高到低:Al >Mg>Na |
| C.晶格能由大到小: NaF> NaCl> NaBr>NaI |
| D.氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4 |
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。其中下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是()
| A.该物质的分子式为SN | B.该物质的分子中既有极性键又有非极性键 |
| C.该物质具有很高的熔、沸点 | D.该物质与化合物S2N2互为同素异形体 |
冶金工业上常用电解熔融MgCl2而不用电解MgO的方法制取镁,其原因是()
| A.熔融的MgO不导电 | B.MgO分子间作用力很大 |
| C.MgO熔点高 | D.MgO属原子晶体 |
下列说法正确的是()
| A.金刚石晶体中,碳原子数与C—C键数之比为1:2 |
B.720g C60晶体含有NA个如图中晶胞单元 |
| C.离子晶体中每个离子周围均吸引着6个带相反电荷的离子 |
| D.Cu的堆积方式是面心立方最密堆积,配位数是8 |
下列物质的性质与氢键无关的是()
| A.冰的密度比液态水的密度小 | B.NH3易液化 |
| C.H2Se沸点比H2S的沸点高 | D.NH3极易溶于水 |