右上图是一原电池的装置,关于它的说法正确的是 
| A.装置中铜是负极 |
| B.铜表面的反应为:2H++2e-=H2↑ |
| C.电流的方向是从铁经导线流向铜 |
| D.构成原电池后,铁与硫酸铜的反应速率加快 |
反应2X(g)+Y(g)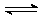 2Z(g)+热量,在不同温度(T1和T2
2Z(g)+热量,在不同温度(T1和T2 )及压强(p1和p2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下述判断正确的是:
)及压强(p1和p2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下述判断正确的是: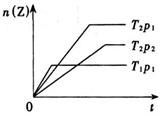
| A.T1<T2,p1<p2 | B.T1<T2,p1>p2 |
| C.T1>T2,p1>p2 | D.T1>T2,p1<p2 |
某温度下,浓度都是1 mol·L-1的两种气体X2和Y2,在密闭容器中反应生成气体Z,反应平衡时,测得物质的浓度分别为:c(X2)=0.4 mol·L-1,c(Y2)=0.8 mol·L-1,c(Z)=0.4 mol·L-1,则该反应的反应式可表示为:
A.X2+2Y2 2XY2 2XY2 |
B.2X2+Y2 X2Y X2Y |
C.3X2+Y2 2X3Y 2X3Y |
D.X2+3Y2 2XY3 2XY3 |
设C+CO2="2CO" △H>0的反应速率为V1;N2+3H2=2NH3△H<0的反应速率为V2。若升温,V1和V2的变化可能是:
| A.同时增大 | B.同时减少 |
| C.V1增大、V2减少 | D.V1减少、V2增大 |
可逆反应2SO2 + O2  2SO3,如果SO2的起始浓度为2 mol/L ,2min后SO2的浓度为1.8mol/L,则用SO2的浓度变化表示的反应速率为:
2SO3,如果SO2的起始浓度为2 mol/L ,2min后SO2的浓度为1.8mol/L,则用SO2的浓度变化表示的反应速率为:
| A.1mol/(L·min) | B.0.9mol/(L·min) |
| C.0.2mol/(L·min) | D.0.1mol/(L·min) |
已知下列数据: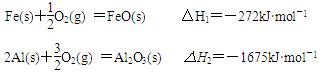
 则:2Al(s) +3FeO(s) = Al2O3(s) + 3Fe(s) 的 △H3是:
则:2Al(s) +3FeO(s) = Al2O3(s) + 3Fe(s) 的 △H3是:
| A.+859 kJ·mol-1 | B.-859 kJ·mol-1 |
| C.-1403 kJ·mol-1 | D.-2491 kJ·mol-1 |