已知反应A2(g)+2B2(g) 2AB2(g) △H<0,下列说法正确的是:
2AB2(g) △H<0,下列说法正确的是:
| A.升高温度,正向反应速率增加,逆向反应速率减小 |
| B.升高温度反应速率增加,从而缩短达到平衡的时间 |
| C.达到平衡后,降低温度或增大压强都有利于该反应平衡正向移动 |
| D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动 |
下列离子方程式表达正确的是( )
| A.等体积,等物质的量浓度的NaHCO3溶液和Ca(OH)2溶液混合:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| B.FeI2溶液中通入少量氯气:2Fe2++Cl2= 2Fe3++2Cl- |
C.CH3COONH4的电离:CH3COONH4 NH4++CH3COO- NH4++CH3COO- |
| D.用食醋除去水瓶中的水垢:CO32-+2CH3COOH==2CH3COO-+CO2↑+H2O |
NA代表阿伏加德罗常数,下列叙述错误的是()
| A.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子 |
| B.1 mol羟基中电子数为10NA |
| C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
| D.常温下,1 L 0.1 mol·L-1的NH4NO3溶液中氮原子数为0.2NA |
下列说法正确的是()
| A.在空气质量日报中CO2含量属于空气污染指数 |
| B.碘盐中的碘可以直接用淀粉检验 |
| C.碳酸氢钠可以用于治疗胃酸过多 |
| D.硫酸氢钠属于盐类,其水溶液显中性 |
现有乙炔、乙醛、乙二醇三种蒸汽的混合物,已知含C量为a%,则氢的含量为
A.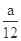 % % |
B.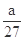 % % |
C.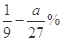 |
D.无法计算 |
下表中所列的都是烷烃,它们的一卤取代物均只有一种,分析下表中各项的排布规律,按此规律排布第6项应为:
| 1 |
2 |
3 |
4 |
5 |
6 |
…… |
| …… |
C2H6 |
C5H12 |
C8H18 |
…… |
…… |
A.C26H54 B.C20H42 C.C17H36 D.C14H30