下列说法正确的是( )
| A.1 molH2的质量是1 g |
| B.1 mol HCl的质量是36.5 g·mol-1 |
| C.Cl2的摩尔质量等于它的相对分子质量 |
| D.硫酸根离子的摩尔质量是96 g·mol-1 |
下列操作或装置能达到实验目的的是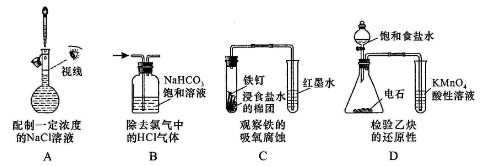
一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是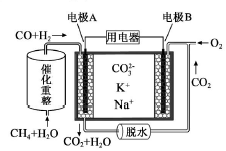
A.反应CH4+H2O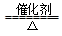 3H2+CO,每消耗1molCH4转移12mol e- 3H2+CO,每消耗1molCH4转移12mol e- |
| B.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- |
| C.电池工作时,CO32-向电极B移动 |
| D.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O |
纯净物X、Y、Z转化关系如图所示,下列判断正确的是
| A.Y不可能是氢气 |
| B.X可能是金属铜 |
| C.Z可能是氯化钠 |
| D.Z可能是三氧化硫 |
下列物质见光不会分解的是
| A.HClO | B.NH4Cl | C.HNO3 | D.AgNO3 |
某化合物由两种单质直接反应生成,将其加入Ba(HCO3)2溶液中同时有气体和沉淀产生。下列化合物中符合上述条件的是
| A.AlCl3 | B.Na2O | C.FeCl2 | D.SiO2 |