分类方法在化学学科发展中起到了非常重要的作用。下列分类标准合理的是:①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等;②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液;④根据水溶液能否导电可将物质分为电解质和非电解质
| A.①③ | B.② | C.①②④ | D.①②③④ |
常温下,下列溶液中与1×10-5mol/L的NaOH溶液pH相同的是()
| A.把pH=6的盐酸稀释1000倍 |
| B.把pH=8的NaOH溶液稀释10倍 |
| C.把10mL 1×10-5mol/L的H2SO4溶液与10mL 4×10-5mol/L的NaOH溶液相混合 |
| D.把c(OH-)=10-5mol/L的NaOH溶液10mL加到100mL浓度为10-4mol/L的NaOH溶液中 |
25 ℃ 时,水的电离达到平衡:H2O H++OH- ΔH > 0,下列叙述正确的是()
H++OH- ΔH > 0,下列叙述正确的是()
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
| C.向水中加入少量固体NaOH,平衡逆向移动,c(H+)降低,KW减小 |
| D.将水加热,KW增大,pH不变 |
下表是常温下某些一元弱酸的电离常数:
| 弱酸 |
HCN |
HF |
CH3COOH |
HNO2 |
| 电离常数 |
6.2×10-10 |
6.8×10-4 |
1.8×10-5 |
6.4×10-4 |
物质的量浓度均为0.1 mol·L-1的下列溶液中,pH由大到小的顺序是()
A.HCN>HNO2>CH3COOH>HF B.HF>HNO2>CH3COOH>HCN
C.HCN>CH3COOH>HNO2>HF D.HCN>CH3COOH>HF>HNO2
下列事实,不能用勒夏特列原理解释的是()
A.氨水中加酸,NH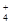 的浓度增大 的浓度增大 |
| B.合成氨工业中不断从反应混合物中液化分离出氨气 |
| C.实验室中常用排饱和食盐水的方法收集Cl2 |
| D.合成氨控制在500 ℃左右的温度 |
常温下用pH试纸测定某溶液的pH,如果将pH试纸用蒸馏水润湿后,再把待测液滴到pH试纸上,跟比色卡对照,测得pH=6。则此溶液的实际pH()
| A.大于6 | B.小于6 | C.等于6 | D.大于7 |