已知有如下反应:①2Fe3++2I-===2Fe2++I2 ②2Fe2++Br2===2Fe3++2Br-
③2Fe(CN)+I2===2Fe(CN)+2I-,试判断氧化性强弱顺序正确的是
| A.Fe3+>Br2>I2>Fe(CN) | B.Br2>I2>Fe3+>Fe(CN) |
| C.Br2>Fe3+>I2>Fe(CN) | D.Fe(CN)>Fe3+>Br2>I2 |
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的不可能是 ( )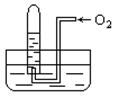
| A.N2与NO2的混和气体 | B.O2与NO2的混和气体 |
| C.NO与NO2的混和气体 | D.NO2一种气体 |
在NO2与水的反应中,水 ( )
| A.是还原剂 | B.是氧化剂 |
| C.既是氧化剂又是还原剂 | D.既不是氧化剂又不是还原剂 |
起固氮作用的化学反应的是: ( )
| A.工业上用氮气和氢气合成氨气 | B.一氧化氮与氧气反应生成二氧化氮 |
| C.氨气经催化氧化生成一氧化氮 | D.由氨气制化肥碳酸氢铵和硫酸铵 |
下列说法错误的是 ( )
| A.原子晶体中只存在非极性共价键 |
| B.分子晶体的状态变化,只需克服分子间相互作用 |
| C.金属晶体通常具有导电、导热和良好的延展性 |
| D.离子晶体在熔化状态下能导电 |
下列说法正确的是 ( )
| A.用乙醇或CCl4可提取碘水中的碘单质 |
| B.NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同 |
| C.24Mg32S晶体中电子总数与中子总数之比为1∶1 |
| D.H2S和SiF4分子中各原子最外层都满足8电子结构 |