(1)写出下列反应的离子方程式:
①纯碱和盐酸反应
②少量二氧化碳通入澄清石灰水  ③氧化铁和盐酸
③氧化铁和盐酸 反应
反应 

(2)写出符合下 列离子反应的化学方程式:
列离子反应的化学方程式:
①CO32- +Ba2+ = BaCO3↓
②Cu2+ +Fe =" Cu" + Fe2+
有a、b两个等体积且极易导热的密闭容器,a保持容积不变,b中的活塞可上下移动,以保持内外压强相等。在相同条件下将3mol A,1mol B分别同时混合于a、b两容器中,发生反应:3A(g)+B(g) 2C(g)+D(g)
2C(g)+D(g)
(1)达到平衡时,a中A的浓度为M mol/L。A的转化率为N,b中A的浓度为m mol/L,A的转化率为n,则M____m;N_____n(填>、<、=、无法比较)
(2)保持温度不变,按下列配比分别充入a、b两容器,达平衡后,a中A的浓度为M mol·L-1的是
A 6mol A+2mol B B 3mol A+2mol C C 2mol C+1mol B+1mol D
D 2mol C+1mol D E 1.5mol C+0.5mol B+1mol C+0.5mol D
氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示)。
(2)负极反应式为 。
(3)电极表面镀铂粉的原因为
2A B + C在某一温度时,达到平衡。
B + C在某一温度时,达到平衡。
(1)若温度升高,平衡向正反应方向移动,则正反应是___________反应(填放热或吸热);
(2)若B为固体,降低压强平衡向逆反应方向移动,则A呈___________态;
(3)若A是气态时,加压时,平衡不移动,则B为_________态,C为__________态;
(4) 若A、B、C均为气体,加入催化剂,平衡___________移动(填正向、逆向、不)
由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:。
下图所示实验中,A、B中的电极为多孔铂电极,c、d为夹在经Na2SO4溶液浸湿的滤纸条上的铂夹,a、b为电源的两极。将A、B中充满KOH溶液后倒立于盛有KOH溶液的水槽中,断开开关K1,闭合K2、K3,通以直流电。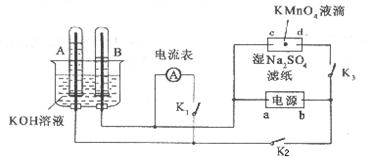
请回答下列问题:
(1) a为直流电源极。
(2) 滤纸上(实验开始时中央滴有KMnO4液滴)的明显现象为;
(3) 写出电极反应式:A极:;C极:。
(4) 若经电解一段时间后,A、B中均有气体包围电极,此时切断K2、K3,闭合K1,则电流表的指针是否发生偏转,说明你的理由。