下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A.0.1 mol /L的(NH4)2SO4溶液中:c (SO42—)> c (NH4+ )> c (H+)> c (OH—) |
| B.0.2 mol /L的Na2CO3溶液中:c (OH—)= c (HCO3—)+ c (H+)+ c (H2CO3) |
| C.0.1 mol /L的NH4Cl溶液与0.05 mol L-l的NaOH溶液等体积混合,其混合溶液中:c (Cl-) > c (NH4+ ) > c (Na+ ) > c (H+) > c (OH-) |
| D.c (NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4C1溶液中: |
c [(NH4)2SO4] < c [(NH4)2CO3] < c (NH4C1)
室温下,pH相差1的两种一元碱溶液A和B,分别加水稀释时,溶液的pH变化如图所示。下列说法正确的是()
A.稀释前两溶液中H+浓度的大小关系:A=10B
B.稀释前,A溶液中由水电离出的OH-的浓度大于10-7 mol/L
C.取等体积M点的A、B两种碱液加入同浓度的硫酸溶液至恰好完全反应时,
所消耗酸溶液的体积相同
D.用醋酸中和A溶液至恰好完全反应时,溶液的pH不一定大于7
下列溶液中微粒浓度关系一定正确的是()
| A.将水加热到100℃,pH=6:c(H+)>c(OH-) |
| B.室温下,pH=7的醋酸和醋酸钠的混合溶液中:c(CH3COO-)>c(Na+) |
| C.0.1mol·L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) |
| D.同浓度的三种溶液:①CH3COONH4②NH4Cl③NH3·H2O中,c(NH4+)由大到小的顺序是②③① |
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:
MgSO4(s) + CO(g)  MgO(s) + CO2(g) +SO2(g)△H>0
MgO(s) + CO2(g) +SO2(g)△H>0
该反应在恒容密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y的值随x变化趋势合理的是()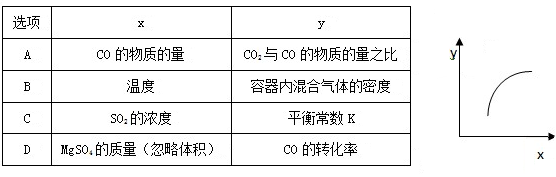
热激活电池可用作火箭、导弹的工作电。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池的总反应方程式为:PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb。下列有关说法正确的是
| A.正极反应式:Ca +2Cl--2e-=CaCl2 |
| B.放电过程中,Li+向负极移动 |
| C.每转移0.1mol电子,理论上生成20.7gPb |
| D.常温时,在正负极间接上电流表或检流计,指针不偏转 |
迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如下图。下列叙述正确的是()
| A.迷迭香酸属于芳香烃 |
| B.1mol迷迭香酸最多能和9mol氢气发生加成反应 |
| C.迷迭香酸可以发生水解反应、取代反应和酯化反应 |
| D.lmol迷迭香酸最多能和含5mol NaOH的水溶液完全反应 |