已知多元弱酸在水溶液中的电离是分步进行的,且第一步电 离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度……
离程度远大于第二步电离程度,第二步电离程度远大于第三步电离程度……
今有HA、H2B、H3C三种一元、二元、三元弱酸,
根据“较强酸 + 较弱酸盐 = 较强酸盐 + 较弱酸”的反应规律,它们之间能发生下列反应:
① HA + HC2-(少量)= A- + H2C-;
② H2B(少量)+2A- = B2- + 2HA;
③ H2B(少量)+ H2C- = HB- + H3C
回答下列问题:
(1)相同条件下,HA、H2B、H3C三种酸中酸性最强的是_________。
(2)A-、B2-、C3-、HB-、H2C-、HC2-六种离子中,最易结合质子(H+)的是_____,最难结合质子的是_____。
(3)完成下列反应的离子方程式
④ H3C + A-:_____________________;⑤ HB- + A-:______________________;
⑥ H3C + B2-:_____________________。
已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出13种元素的X的数值:
| 元素 |
Al |
B |
Be |
C |
Cl |
F |
Li |
| X数值 |
1.5 |
2.0 |
1.5 |
2.5 |
2.8 |
4.0 |
1.0 |
| 元素 |
Mg |
Na |
O |
P |
S |
Si |
|
| X数值 |
1.2 |
0.9 |
3.5 |
2.1 |
2.5 |
1.7 |
试结合元素周期律知识完成下列问题:
(1)经验规律:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AIBr3中的化学键类型是。
(2)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系。
简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系
。
(3)某化合物分子中含有S-N键,该共用电子对偏向于原子(填元素符号)。
1994年度诺贝尔化学奖授予为研究臭氧作出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。臭氧分子的结构如图,呈V型,两个O-O键的夹角为116.5º,三个原子以一个O原子为中心,与另外两个氧原子分别构成共价键;中间O原子提供2个电子,旁边两个O原子各提供一个电子,构成一个特殊的化学健―三个O原子均等地享有这4个电子。(如右图所示)。请回答:
(1)臭氧与氧气的关系是______________。
(2)选出下列分子与O3分子的结构最相似的是()
| A.H2O | B.CO2 | C.SO2 | D.BeCl2 |
(3)分子中某原子没有跟其他原子共用的价电子对叫孤对电子,那么O3分子有 对孤对电子。
(4)O3具有强氧化性,它能氧化PbS为PbSO4,而O2不能,试配平:
_____PbS + _____O3 ——_____PbSO4 + _____O2;
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED)。目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、lnGaN(氮化铟镓)为主。砷化镓的品胞结构如右图。试回答:
(1)镓的基态原子的电子排布式是。
(2)砷化镓品胞中所包含的砷原子(白色球)个数为,与同一个镓原子相连的砷原子构成的空 间构型为。
间构型为。
(3)下列说法正确的是(填字母)。
A.砷化镓品胞结构与NaCl相同
B.第一电离能:As>Ga
C.电负性:As>Ga
D.砷化镓晶体中含有配位键
E.GaP与GaAs互为等电子体
(4)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是。
(5)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为。
B.乙酸乙酯的实验室和工业制法常采用如下反应:
CH3COOH+C2H5OH CH3COOC2H5+H2O
CH3COOC2H5+H2O
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH;
②部分有机物的沸点:
| 试剂 |
乙醚 |
乙醇 |
乙酸 |
乙酸乙酯 |
| 沸点(℃) |
34.5 |
78.5 |
117.9 |
77 |
请回答下列问题:
(1)浓硫酸的作用是,球形干燥管的作用是。
(2)用如图所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为、
等。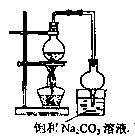
(3)实验所得到的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,除去;再进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作此反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)。
| 同一反应时间 |
同一反应应温度 |
||||
反应温度/ ℃ ℃ |
转化率(%) |
选择性(%)* |
反应时间/h |
转化率(%) |
选择性(%)* |
| 40 |
77.8 |
100 |
2 |
80.2 |
100 |
| 60 |
92.3 |
100 |
3 |
87.8 |
100 |
| 80 |
92.6 |
100 |
4 |
92.3 |
100 |
| 120 |
94.5 |
98.7 |
6 |
93.0 |
100 |
| *选择性100%表示反应生成的产物全部是乙酸乙酯和水 |
①根据表中数据,下列(填字母)为该反应的最佳条件。
a.120℃,4h b.80℃,2h c.60℃,4h d.40℃,3h
②当反应温度达到120℃时,反应选抒性降低的原因可能为。
巨豆三烯酮(F)是一种重要的香料,其合成路线如下:
(1)化合物C含有的官能团的名称为。
(2)化合物F的结构简式是。
(3)在上述转化过程中,步骤②的目的是 ,写出步骤②的化学方程式。
,写出步骤②的化学方程式。
(4)写出符合下列条件的D的一种同分异构体的结构简式。
a.属于芳香族化合物;
b.核磁共振氢谱显示,分子中有4种化学环境不同的氢原子;
c.1mol该物质最多可消耗2molNaOH
d.能发生银镜反应。
(5)兔耳草醛( )也是一种重要的香料,主要用于食品、化妆品等工业中。请设计合理方案,以对异丙基苯甲醛(
)也是一种重要的香料,主要用于食品、化妆品等工业中。请设计合理方案,以对异丙基苯甲醛(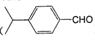 )和丙醛为原料合成兔耳草醛(用合成路线流程图表示,并注明反应条件)。
)和丙醛为原料合成兔耳草醛(用合成路线流程图表示,并注明反应条件)。
提示:①2CH3CHO CH3CH(OH)CH2CHO
CH3CH(OH)CH2CHO CH3CH=CHCHO
CH3CH=CHCHO
②合成过程中无机试剂任选;
③合成路线流程图示例如下:
。
硫酸铜是一种重要的化工原料,工业上常用硫酸为原料来制备硫酸铜。
(1)工业上生产硫酸过程中,焙烧硫铁矿时产生的废渣是一种二次资源。
①为了从废渣中磁选获得品位合格的铁精矿,高温下利用CO使弱磁性Fe2O3转化为强磁性Fe3O4。写出该反应的化学方程式;实验发现:CO太多或太少都会导致磁铁矿产率降低,原因是。
②氯化焙烧工艺是将废渣用氯化钙水溶液调和、成球、高温焙烧,废渣中SiO2与CaCl2等在高温下反应放出HCl,HCl与金属氧化物等反应生成氯化物。反应生成的各金属氯化物以气态形式逸出,进而回收有色金属和回返氯化钙溶液。写出氯化焙烧工艺中生成HCl的化学方程式。
(2)测定硫酸铜品体中结品水含量的实验步骤为:
步骤1:准确称量一个洁净、干燥的坩埚;
步骤2:将一定量的硫酸铜晶体试样研细后,放入坩埚中称重
步骤3:将盛有试样的坩埚加热,待晶体变成白色粉末时,停止加热;
步骤4:将步骤3中的坩埚放入干燥器,冷却至室温后,称重:
步骤5:;
步骤6:根据实验数据计算硫酸铜晶体试样中结晶水的质量分数。
请完成实验步骤5。
(3)已知硫酸铜品体受热可以逐步失去结品水,温 度升高还町以分解生成铜的氧化物。观取25.0g CuSO4·5H2O品体均匀受热,缓慢升温至1200℃并恒温1小时,实验测得固体残留率(剩余固体的质量/原始固体质量)与温度的关系如下图所示:
度升高还町以分解生成铜的氧化物。观取25.0g CuSO4·5H2O品体均匀受热,缓慢升温至1200℃并恒温1小时,实验测得固体残留率(剩余固体的质量/原始固体质量)与温度的关系如下图所示: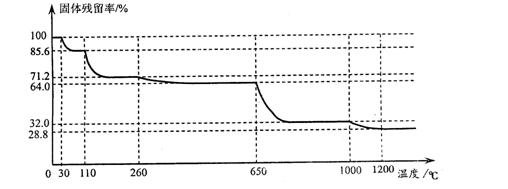
在110℃时所得固体的成分为;在1200℃并恒温1小时,反应所 得气态产物除去水后,物质的量为。(填字母)
得气态产物除去水后,物质的量为。(填字母)
| A.0 mol | B.0.1mol | C.0.125mol | D.大于0.125mol |