a mL三种气态烃的混合物和足量的氧气混合点燃爆炸后,恢复到原来的状态(常温常压),气体体积共缩小2 amL。则三种烃可能的组合是
| A.CH4、C2H4、C3H4任意体积比 |
| B.CH4、C3H6、C2H2保持C3H6∶C2H2=1∶ 2(物质的量之比) |
| C.C2H6、C4H6、C2H2同条件下体积比为2∶1∶1 |
| D.C3H8、C4H8、C2H2质量比为11:14:16 |
某有机物是药物生产的中间体,其结构简式如图。下列有关叙述不正确的是
| A.该有机物与浓溴水可发生取代反应 |
| B.该有机物与浓硫酸混合共热可发生消去反应 |
| C.1 mol该有机物与足量NaOH溶液反应最多消耗4 mol NaOH |
| D.该有机物经催化氧化后与新制氢氧化铜悬浊液共热生成砖红色沉淀 |
下列叙述正确的是
| A.锥形瓶可用作加热的反应器 |
| B.室温下,不能将浓硫酸盛放在铁桶中 |
| C.配制溶液定容时,仰视容量瓶刻度会使溶液浓度偏高 |
| D.用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低 |
化学与社会、生产、生活紧切相关,下列说法正确的是
①石英只可用于生产光导纤维,且常温下不与强酸反应;
②次氯酸钠溶液可用于环境的消毒杀菌;
③黑火药由硫黄、硝石、木炭三种物质按一定比例混合制成;
④用铜片在加热的条件下就可鉴别浓硫酸和稀硫酸;
⑤70mL的H2S和90mL的O2混合点燃后恢复到原状况可产生70mL的SO2;
⑥将过量CO2气体通入水玻璃中可生成硅酸和纯碱
| A.①②④⑤ | B.①②③④ | C.②④⑥ | D.②③④ |
25℃时,几种弱酸的电离常数如下:
| 弱酸的化学式 |
CH3COOH |
HCN |
H2S |
| 电离常数(25℃) |
1.8×10-5 |
4.9×10-10 |
K1=1.3×10-7 K2=7.1×10-15 |
25℃时,下列说法正确的是
A.等物质的量浓度的各溶液pH关系为:pH(CH3COONa)> pH(Na2S) > pH(NaCN)
B.a mol/LHCN溶液与b mol/LNaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于或等于b
C.NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)
D.某浓度的NaCN溶液的pH=d,则其中由水电离出的c(OH-)=10-dmol/L
在某一恒温体积可变的密闭容器中发生如下反应:A(g)+B(g) 2C(g) △H<0。t1 时刻达到平衡后,在t2 时刻改变某一条件,其反应过程如图所示。下列说法正确的是
2C(g) △H<0。t1 时刻达到平衡后,在t2 时刻改变某一条件,其反应过程如图所示。下列说法正确的是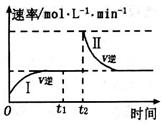
A.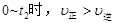 |
| B.I、Ⅱ两过程达到平衡时,A的体积分数I﹥II |
C.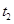 时刻改变的条件是向密闭容器中加C 时刻改变的条件是向密闭容器中加C |
| D.I、II两过程达到平衡时,平衡常数I﹤II |