室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是 ( )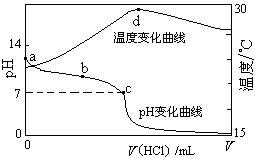
| A.a点由水电离出的c(H+)=1.0×10-14mol/L |
| B.b点:c(NH4+)+c(NH3·H2O)=c(Cl-) |
| C.c点:c(Cl-)= c(NH4+) |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
下列说法正确的是()
| A.铝在空气中耐腐蚀,所以铝是不活泼金属 |
| B.点燃的镁条插入盛有CO2的集气瓶中,立即熄灭 |
| C.铝在高温下能还原锰、铁、铬等金属氧化物得到金属 |
| D.因为镁和铝在空气中都能形成氧化膜,所以镁铝都不能溶于浓硝酸 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是()
| A.28g氮气所含有的原子数目为NA |
| B.化学反应中1mol金属镁变成镁离子时失去电子数目为2NA |
| C.标准状况下,22.4L水中含有个水分子NA |
| D.标准状况下,22.4L氯化氢所含的原子数为NA |
下列物质的分子中,既有σ键又有π 键的是
| A.N2 | B.HClO | C.CH4 | D.C2H6 |
下列元素的电负性最大的是:
| A.Na | B.S | C.O | D.C |
下列各组物质中,都是由极性键构成为极性分子的一组的
| A.CH4 和 H2O | B.CO2和 HCl |
| C.NH3 和 H2S | D.HCN 和 BF3 |