Ⅰ.A、B、C、D、E为短周期的五种元素,它们原子序数依次递增,B是构成有机物的主要元素;A与C可形成10电子化合物W,它可使紫色石蕊试液变蓝;D元素的原子最外层电子数是其次外层电子数3倍;E是同周期元素中原子半径最大的元素;A、B、C、D可形成化合物X,在X晶体中阳离子与阴离子个数比为1∶1;A、D、E可形成化合物Y。A、C、D可形成离子化合物Z。回答下列问题:
⑴Y的电子式: ;W的空间构型: ;
;
⑵写出Z的水溶液中各离子浓度由大到小的顺序: ;
⑶写出常温下X与足量的Y在溶液中反应的离子方程式: ;
⑷写出由A、B、D形成的化合物在一定条 件下制取常见果实催熟剂的化学方程式:
件下制取常见果实催熟剂的化学方程式:
⑸用石墨为电极电解Y的水溶液时,阳极的电极反应式为 ,一段时间后溶液的pH (从“增大”“减小”或“不变”中选填).
Ⅱ.南昌大学研发出一种新型纳米锂电池,已跻身国内领先地位。以下是某种锂离子的电池反应方程式 :
: (C6Li表示锂原子嵌入石墨形成的复合材料,LiMO2表示含锂的过渡金属氧化物)回答:
(C6Li表示锂原子嵌入石墨形成的复合材料,LiMO2表示含锂的过渡金属氧化物)回答:
⑴锂电池放电时的负极反应为:C6Li -xe-=C6Li1-x+xLi+,则正极反应为: ;⑵电池放电时若转移1mol e-,消
-xe-=C6Li1-x+xLi+,则正极反应为: ;⑵电池放电时若转移1mol e-,消 耗的负极材料 g。
耗的负极材料 g。
实验室中需要220mL0.5mol/L H2SO4,现用98%浓硫酸(密度为1.84g/cm3)稀释配制。
(1)本实验室中需要的仪器是 。
(2)要将浓硫酸在 中稀释,稀释时的操作方法是 。
(3)必须将稀释后的硫酸 后再移液,原因是 ,否则,所配制的稀硫酸浓度会 (偏高、偏低、无影响)。
按要求填空:
(1)Fe(OH)2在空气中变质的化学方程为:_____________________________。
(2)漂白粉在空气中久置会变质,变质过程中既有非氧化还原反应又有氧化还原反应,其中氧化还原反应的方程式为:_______________________________。
(3)实验室制备氨气的反应方程式为:______________________,收集氨气时,在试管口放一小团棉花其作用是________________,用_______________试纸检验氨气是否收集满。
(4)将CaMg3Si4O12改写为氧化物的形式:_______________________。
某无色透明溶液可能存在Na+、Fe3+、Ba2+、NO3-、CO32-、HCO3-、SO42-中的几种离子,现有如下操作:
Ⅰ、取适量该溶液加入CaCl2溶液无沉淀,继续滴加盐酸产生无色无味的气体。
Ⅱ、另取该溶液滴加一定量的NaOH溶液有白色沉淀生成。
试回答下列问题:
①该溶液中一定存在的离子有______________,一定不存在的离子_____________。
②用一个离子方程式表示操作②的实验现象:__________________________。
(A)【化学—物质结构与性质】
物质中铁含量的测定方法是多种多样的。
I.土壤中铁含量的测定是先将Fe3+还原为Fe2+,然后使Fe3+与邻啡罗啉 结合显橙红色,再用比色法测定。其中涉及反应:4FeCl3 + 2NH2OH·HCl ="==" 4FeCl2 + N2O↑+ 6HCI + H2O
结合显橙红色,再用比色法测定。其中涉及反应:4FeCl3 + 2NH2OH·HCl ="==" 4FeCl2 + N2O↑+ 6HCI + H2O
(1)基态Fe2+的核外电子排布式为。
(2)羟胺(NH2OH)中采用sp3杂化的原子是;
羟胺极易溶于水,主要原因是。
(3)羟胺的组成各元素中,元素的第一电离能(I1)由大到小的顺序为(用元素符号表示)。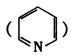
(4)吡啶和邻啡罗啉都是含氮的有机物,l mol吡啶中含有σ键的物质的量为mol。
Ⅱ.奶粉中铁含量的测定是在酸性介质中使Fe3+与K4Fe(CN)6生成普鲁士蓝(Ⅱ)(化学式为Fe4[Fe(CN)6]3),再用光度法测定铁的含量。反应原理:3K4Fe(CN)6+4FeCl3 ="==" Fe4[Fe(CN)6]3↓+12KCl
(5)Fe4[Fe(CN)6]3是一种配合物,其中含有的化学键有;
a.共价键
b.氢键
c.配位键
d.金属键
e.离子键
(6)若K4 Fe(CN)6和FeCl3的物质的量按某种比例发生反应,可生成普鲁士蓝(I),其晶胞结构如下图所示:据此判断普鲁士蓝(I)中n(K+):n(Fe3+):n (Fe2+):n (CN—)= 。
目前机动车使用的电池品种不少,其中铅蓄电池的使用量最大。
I.铅蓄电池的电极材料分别是Pb和PbO2,电解质溶液为稀硫酸。铅蓄电池充放电的总反应方程式为:
PbO2+Pb+2H2SO4 2PbSO4+2H2O,
2PbSO4+2H2O,
请根据上述情况判断:
(1)电池的负极材料是。
(2)充电时,铅蓄电池阳极的电极反应式为。
Ⅱ.铅蓄电池使用量的急速增加引起铅污染日益严重,工业上从废铅蓄电池的铅膏回收铅的一种工艺流程如下:
请回答下列问题:
(3)为提高步骤①的化学反应速率,你认为可采取的措施是(写一条即可)。
(4)写出步骤①中PbSO4转化为PbCO3反应的平衡常数表达式:K =。
(5)步骤①中发生氧化还原反应的化学方程式为。
(6)步骤③从母液可获得的副产品为(写化学式)。
(7)已知:PbCO3在一定条件下可制得PbO,PbO通过进一步反应可制得Pb,写出一个由PbO生成Pb的化学方程式:。