某化合物的结构(键线式)及球棍模型如下;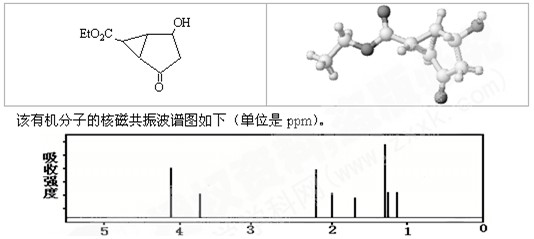
下列关于该有机物的叙述正确的是
| A.该有机物不同化学环境的氢原子有8种 | B.该有机物属于芳香族化合物 |
| C.键线式中的Et代表的基团为-CH3 | D.该有机物不可能发生消去反应 |
短周期元素W、X、Y、和Z的原子序数依次增大,元素W是制造一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是电子层数的2倍。下列说法中错误的是:()
| A.元素W、X的氯化物中,各原子均满足8电子的稳定结构。 |
| B.元素X与氢形成的原子比为1:1的化合物有很多种 |
| C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 |
| D.元素Z可与元素X形成共价化合物XZ2 |
某溶液中可能含有Na+、Ca2+、Br-、CO32-、I-、SO32-六种离子中的几种。①在该溶液中滴加足量氯水后,有气泡产生、溶液呈橙黄色;②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成;③橙黄色溶液不能使淀粉溶液变蓝。据上述实验事实推断,在该溶液中肯定存在的离子组是 ( )
| A.Na+、Br-、CO32- | B.Na+、SO32-、I- |
| C.Ca2+、I-、SO32- | D.Ca2+、CO32-、Br- |
关于反应中的先后顺序,下列评价正确的是 ( )
| A.向浓度都为0.1 mol/L 的FeCl3和CuCl2混合溶液加入铁粉,CuCl2首先反应 |
| B.向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH4+首先反应 |
| C.向浓度都为0.1 mol/LNa2 CO3和NaOH溶液通入CO2气体,NaOH首先反应 |
| D.向浓度都为0.1 mol/L 的FeCl3加入质量相同、颗粒大小相同的铁和铜,铜先反应 |
某溶液中含有AlO2-、SO32-、SO42-、Na+,向其中加入Na2O2后,溶液中浓度基本保持不变的离子是 ( )
| A.SO32- | B.Na+ | C.AlO2- | D.SO42- |
美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是()
| A.合金的熔点一般比组分金属低 |
| B.铝钠合金若投入一定量的水中可得无色溶液,则n(Al)≤n(Na) |
| C.铝钠合金投入到足量氯化铜溶液中,会有氢氧化铜沉淀也可能有铜析出 |
| D.若m g不同组成的铝钠合金投入足量盐酸中,放出的H2越多,则铝的质量分数越小 |