下列实验不能达到预期目的的是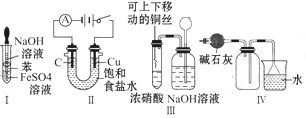
| A.利用Ⅰ制取Fe(OH)2 |
| B.利用Ⅱ装置电解饱和食盐水 |
| C.利用Ⅲ装置进行铜与浓硝酸反应的实验 |
| D.利用Ⅳ装置收集NH3 |
已知NaHSO3溶液呈酸性、NaHCO3溶液呈碱性。现有两瓶浓度均为0.1 mol·L-1的NaHSO3溶液和NaHCO3溶液,溶液中各粒子的物质的量浓度存在下列关系(R表示S或C),其中两个溶液中都存在且正确的是
A.c(Na+)>c(HRO3-)>c(H+)>c(RO32-)>c(OH-)
B.c(Na+)+c(H+)=c(HRO3-)+c (RO32-)+c(OH-)
(RO32-)+c(OH-)
C.c(H+)+c(H2RO3)=c(RO32-)+c(OH-)
D.两溶液中c(Na+)、c(HRO3-)、c(RO32-)分别相等
下列反应的离子方程式正确的是
A.醋酸铵溶液和盐酸反应 CH3COONH4+H+ CH3COOH+NH4+ CH3COOH+NH4+ |
B.硫化钠溶液呈碱性 S2-+2H2O H2S+2OH- H2S+2OH- |
| C.硫酸铝溶液和小苏打溶液反应 Al3++3HCO3-==3CO2↑+Al(OH)3↓ |
D.向稀氨水中加入稀盐酸 OH-+H+ H2O H2O |
有些化学反应 反应速率很慢且副反应较多,测定这些反应的焓变可运用
反应速率很慢且副反应较多,测定这些反应的焓变可运用
| A.阿伏加德罗定律 | B.勒夏特列原理 | C.盖斯定律 | D.质量守恒定律 |
欲使0.1mol/L的 NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-) 都减少,其方法是
| A.通入二氧化碳气体 | B.加入氢氧化钠固体 |
| C.通入氯化氢气体 | D.加入饱和石灰水溶液 |
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)  Si(s)+4HCl(g)
Si(s)+4HCl(g) mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下列叙述正确的是
| A.反应过程中,若增大压强能提高SiCl4的转化率 |
| B.若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为Q kJ |
| C.反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L·min) |
| D.当反应吸收热量为0.025Q kJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应 |