下列方程式书写正确的是
A.HCO3-在水溶液中的电离方程式:HCO3-+H2O H3O++CO32- H3O++CO32- |
| B.H2SO3的电离方程式H2SO3=H++HSO3- |
C.CO32-的水解方程式:CO32-+2H2O H2CO3+2OH- H2CO3+2OH- |
D.Fe3+的水解方程式:Fe3++3H2O Fe(OH)3 ↓+3H+ Fe(OH)3 ↓+3H+ |
下列金属与水反应最剧烈的是
| A.Li | B.Al | C.Rb | D.Ca |
金属钛(22Ti)对人体无毒且惰性,能与肌肉和骨骼生长在一起,有“生物金属”之称。下列关于48Ti和50Ti及钛元素的说法正确的是
| A.原子核外M层都有12个电子 | B.钛元素不是主族元素 |
| C.钛元素的相对原子质量必为49 | D.48Ti和50Ti为同一核素 |
人类将在未来几十年内逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能等太阳能的转换形态),届时人们将适应“低碳经济”和“低碳生活”。下列说法错误的是
| A.煤、石油、天然气都属于碳素燃料 |
| B.发展太阳能经济有助于减缓温室效应 |
| C.菠菜蛋白质“发电”不属于太阳能文明 |
| D.太阳能电池可将太阳能转化为电能 |
下列能源属于可再生能源、一次能源的是
| A.化石能源 | B.氢能 |
| C.乙醇 | D.生物质能源 |
元素氯及其化合物在生产、生活、科研中有广泛的应用。
⑴25℃时,PbCl2固体在不同浓度盐酸(mol·L-1)中的
溶解度(mmol·L-1)如右图。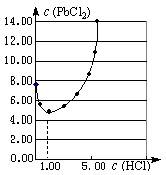
①在制备PbCl2的实验中,洗涤PbCl2固体最好选用。
a.蒸馏水 b.1mol·L-1盐酸
c.5 mol·L-1盐酸 d.10mol·L-1盐酸
②当盐酸的浓度小于1mol·L-1时,随着盐酸浓度的增大, PbCl2的溶解度减小,其原因是。
⑵TCCA广泛用于漂白、杀菌消毒,其学名为三氯均三嗪-2,4,6-三酮,分子式为C3Cl3N3O3。
①TCCA分子具有完全对称的结构,并含有一个六元环,则其结构简式为。
②使用TCCA时,需先将该物质溶解于水,其水解产物之一为C3H3N3O3,另一种产物具有强氧化性,能够杀菌消毒。写出另一种产物的电子式。
⑶高氯酸铵(AP)作为一种优良的固体推进剂被用于导弹和火箭发射。目前,较为先进的制备方法是电解高纯次氯酸得到高纯高氯酸,再与高纯氨进行喷雾反应制成高氯酸铵。写出由次氯酸电解制备高氯酸的阳极反应式:。