在溶液中能大量共存的一组离子或分子是( )
| A.NH4+、H+、NO3-、HCO3- | B.K+ 、Al3+、SO42-、NH3·H2O |
| C.Na+、K+、SO32-、Cl2 | D.Na+ 、CH3COO-、 、OH- 、OH- |
下列图像表达正确的是 ( ) 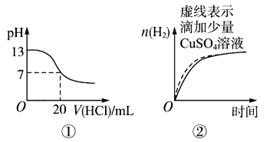
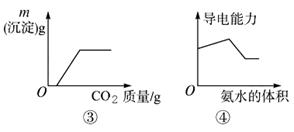
| A.图①表示25 ℃时,用0.1 mol/L盐酸滴定20 mL 0.1mol/L氨水 |
| B.图②表示常温下,等量锌粉分别与两份足量的等体积等浓度的盐酸反应 |
| C.图③表示向CaCl2溶液中通入CO2 |
| D.图④表示向醋酸溶液中滴入氨水 |
为证明某可溶性一元酸(HX)是弱酸,有如下实验方案,其中不合理的是( )
| A.室温下,测0.1 mol/L HX溶液的pH,若pH>1,证明HX是弱酸 |
| B.室温下,测1 mol/L NaX溶液的pH,若pH>7,证明HX是弱酸 |
| C.将等浓度、等体积的HCl和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸 |
| D.相同条件下,对0.1 mol/L的HCl和0.1 mol/L的HX进行导电性实验,若与HX溶液相 |
串联的灯泡较暗,证明HX为弱酸
已知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16 ,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是( )
| A.AgCl>AgI> Ag2CrO4 | B.Ag2CrO4>AgCl>AgI |
| C.AgCl> Ag2CrO4>AgI | D.Ag2CrO4>AgI>AgCl |
下列说法不正确的是()
| A.pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7 |
| B.将等体积pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多 |
| C.向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+) = c(Cl-) |
| D.0.2 mol·L-1的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H+) |
已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1mol/L的NaA
和NaB混合溶液中,下列排序正确的是()
A.c(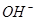 )>c(A-)>c(B-)>c(H+) B.c(OH—)>c(HA)>c(HB)>c(H+)
)>c(A-)>c(B-)>c(H+) B.c(OH—)>c(HA)>c(HB)>c(H+)
C.c(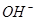 )>c(B-)>c(A-)>c(H+) D. c(
)>c(B-)>c(A-)>c(H+) D. c(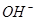 )>c(HB)>c(HA)>c(H+)
)>c(HB)>c(HA)>c(H+)