按要求完成下列各题:
(1)写出乙醛与氢气反应的化学方程式:
。
(2)正丙醇催化氧化反应的化学方程式:
。
(3)丙醛和新制备的银氨溶液的反应:

 。
。
Ⅰ.维生素C的结构简式是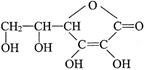 ,它的分子式是______________。由于它能防治坏血病,又称为_________________。在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有__________性;在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到的现象是______________,说明维生素C具有_______________性。
,它的分子式是______________。由于它能防治坏血病,又称为_________________。在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有__________性;在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到的现象是______________,说明维生素C具有_______________性。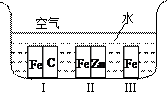
Ⅱ.(1)如右图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号)_______________。
(2)氟氯代烷是一种能破坏臭氧层的物质。在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:
①Cl+O3→ClO+O2②O3→O+O2③ClO+O→Cl+O2
上列的反应的总反应式是________________________,少量氟氯代烷能破坏大量臭氧的原因是___________________________________。
过氧化尿素[CO(NH2)2·H2O2 ]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域。其合成如下: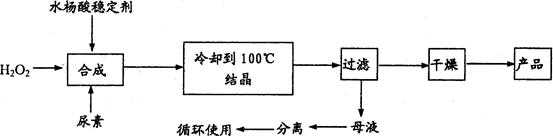
试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25—30℃,其主要原因是___________________________________。
(2)从母液中分离出H2O2和尿素,采用的操作是___________。
(a)盐析过滤(b)分液过滤(c)减压蒸馏结晶(d)常压蒸馏萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000 mol/L KMnO4标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应)。
①KMnO4溶液应盛放在________式(选填:“酸”、“碱”)滴定管中。
②完成并配平方程式:__MnO4-+ ___H2O2+___H+=___Mn2++ ____H2O+________
③根据滴定结果,可确定产品中活性氧的质量分数为:___________。
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”)。
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为_________。
二甲醚(CH3OCH3)和甲醇(CH3OH)被 称为21世纪的新型燃料。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下:
称为21世纪的新型燃料。以CH4和H2O为原料制备二甲醚和甲醇的工业流程如下: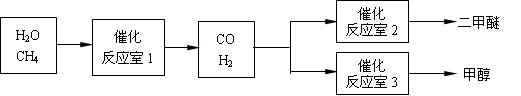
请填空:
(1)在一定条件下,反应室1中发生反应:CH4(g)+H2O(g) CO(g)+3H2(g)△H>0。在其它条件不变的情况下降低温度,逆反应速率将(填“增大”、“减小”或“不变”)。将1.0molCH4和2.0molH2O通入反应室1(假设容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率V(H2)=。
CO(g)+3H2(g)△H>0。在其它条件不变的情况下降低温度,逆反应速率将(填“增大”、“减小”或“不变”)。将1.0molCH4和2.0molH2O通入反应室1(假设容积为100L),10min末有0.1molCO生成,则10min内反应的平均速率V(H2)=。
(2)在一定条件下,已知反应室2的可逆反应除生成二甲醚外还生成了气态水,其化学方程式为。
(3)在压强为0.1MPa条件下,反应室3(容积为VL)中amolCO与2amolH2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)  CH3OH(g),CO的平衡转化率与温度、压强的关系如右图所示,则:
CH3OH(g),CO的平衡转化率与温度、压强的关系如右图所示,则:
① P1P2 (填“<”、“>”或“=")。
②在其它条件不变的情况下,反应室3再增加amolCO
与2amolH2,达到新平衡时,CO的转化率______(填“增大”、“减小”或“不变”。下同。),平衡常数。
③在P1压强下,100℃时,CH3OH(g) CO(g) + 2H2(g)反应的平衡常数为
CO(g) + 2H2(g)反应的平衡常数为
(用含a、V的代数式表示)。
雷诺嗪是治疗慢性心绞痛首选新药。雷诺嗪合成路线如下: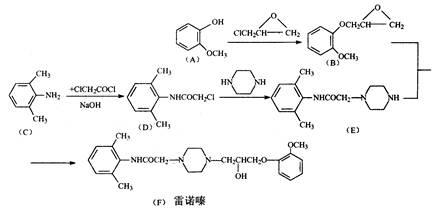
(1)雷诺嗪中含氧官能团,除酰胺键(-NHCO-)外,另两种
 官能团名称:______、_______。
官能团名称:______、_______。
(2)写出满足下列条件A的同分异构体的数目__________。
①A能与FeCl3溶液发生显色反应;②1mol A可与2mol NaOH反应。
(3)C→ D中,加入适量NaOH的作用是:_________________________________。
D中,加入适量NaOH的作用是:_________________________________。
(4)从雷诺嗪合成路线得到启示,可用间二甲苯、ClCH2COCl、(C2H5)NH(无机试剂任用)合成盐酸利多卡因,请在横线上补充反应物,在方框内补充生成物。
已知: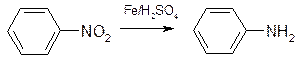
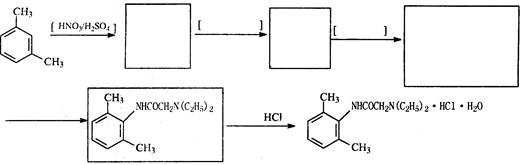
在一定温度下(已知在该温度下,容器内所有物质均为气态),10 L密闭容器中加入5 mol SO2.4 mol O2,经10 min后反应达平衡时有2 mol SO2发生了反应。试计算:
(1)用SO2表示该反应的反应速率;
(2)O2的转化率;
(3)该温度下的平衡常数K(保留三位有效数字)。