下列说法不正确的是
| A.CH3—CH=CH2和CH2=CH2的最简式相同 | B.CH≡CH和C6H6含碳量相同 |
| C.乙二醇和丙三醇为同系物 | D.正戊烷、异戊烷、新戊烷的沸点渐低 |
下列变化需要加入还原剂才能实现的
A.MnO4-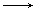 Mn2+ Mn2+ |
B.HCl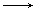 Cl2 Cl2 |
C.Fe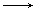 Fe3+ Fe3+ |
D.KClO3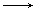 O2 O2 |
铁和水蒸气在高温条件下发生反应3Fe+4H2O(g)  Fe3O4+4H2 ,在此反应中水是
Fe3O4+4H2 ,在此反应中水是
| A.氧化剂 |
| B.还原剂 |
| C.既是氧化剂又是还原剂 |
| D.既不是氧化剂又不是还原剂 |
在碱性溶液中能大量共存且为无色透明溶液的是
| A.K+、Cl-、MnO4-、 SO42- |
| B.Na+、CO32-、NO3-、SO42- |
| C.Na+、NO3-、SO42-、Mg2+ |
| D.Cu2+、NO3-、SO42-、Cl- |
下列反应既是离子反应,又是氧化还原反应的是
| A.氯化钠溶液中滴入硝酸银溶液 |
| B.氢气还原氧化铜 |
| C.铁片置于硫酸铜溶液中 |
| D.一氧化碳的燃烧 |
下列离子方程式中,正确的是
| A.稀硫酸滴在铁片上:2Fe+6H+=2Fe3++3H2↑ |
| B.碳酸氢钠溶液与稀盐酸混合:HCO3-+H+=H2O+CO2↑ |
| C.硫酸铜溶液与氢氧化钠溶液混合:CuS04+20H-=Cu(OH)2↓+SO42- |
| D.硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-=AgCl↓+N03- |